Ενεργά συστατικά: Sunitinib
SUTENT 12,5 mg σκληρά καψάκια
SUTENT 25 mg σκληρά καψάκια
SUTENT 37,5 mg σκληρά καψάκια
SUTENT 50 mg σκληρά καψάκια
Ενδείξεις Γιατί χρησιμοποιείται το Sutent; Σε τι χρησιμεύει;
Το Sutent περιέχει τη δραστική ουσία sunitinib, η οποία είναι αναστολέας πρωτεϊνικής κινάσης. Χρησιμοποιείται για τη θεραπεία του καρκίνου εμποδίζοντας τη δραστηριότητα μιας συγκεκριμένης ομάδας πρωτεϊνών που είναι γνωστό ότι εμπλέκονται στην ανάπτυξη και εξάπλωση των καρκινικών κυττάρων.
Το Sutent θα σας συνταγογραφηθεί μόνο από γιατρό που έχει εμπειρία στη χρήση φαρμάκων για τον καρκίνο.
Το Sutent χρησιμοποιείται για τη θεραπεία ενηλίκων με τους ακόλουθους τύπους καρκίνου:
- Γαστρεντερικός στρωματικός καρκίνος (GIST), ένας τύπος καρκίνου του στομάχου και των εντέρων, σε περιπτώσεις όπου η ιματινίμπη (άλλο αντικαρκινικό φάρμακο) δεν λειτουργεί πλέον ή δεν μπορεί πλέον να ληφθεί.
- Μεταστατικός καρκίνος νεφρού (MRCC), ένας τύπος καρκίνου νεφρού που έχει εξαπλωθεί σε άλλα μέρη του σώματος.
- Παγκρεατικοί νευροενδοκρινικοί όγκοι (pNETs) (όγκοι των κυττάρων που παράγουν ορμόνες του παγκρέατος) που προοδεύουν ή δεν είναι εφικτοί
Το Εάν δεν είστε βέβαιοι για το πώς λειτουργεί το Sutent ή γιατί σας έχει συνταγογραφηθεί αυτό το φάρμακο, ρωτήστε το γιατρό σας.
Αντενδείξεις Όταν το Sutent δεν πρέπει να χρησιμοποιείται
Μην πάρετε το Sutent:
- Εάν είστε αλλεργικοί στο sunitinib ή σε οποιοδήποτε άλλο συστατικό αυτού του φαρμάκου (αναφέρονται στην παράγραφο 6).
Προφυλάξεις κατά τη χρήση Τι πρέπει να γνωρίζετε πριν πάρετε το Sutent
Ενημερώστε το γιατρό σας πριν πάρετε το Sutent:
- Εάν έχετε υψηλή αρτηριακή πίεση. Το Sutent μπορεί να προκαλέσει αύξηση της αρτηριακής σας πίεσης. Ο γιατρός σας μπορεί να ελέγξει την αρτηριακή σας πίεση ενώ παίρνετε το Sutent και θα χρειαστεί να λάβει φάρμακα για τη μείωση της αρτηριακής σας πίεσης εάν είναι απαραίτητο.
- Εάν έχετε ή είχατε διαταραχές του αίματος, προβλήματα αιμορραγίας ή μώλωπες. Η θεραπεία με Sutent μπορεί να εγκυμονεί αυξημένο κίνδυνο αιμορραγίας, αλλαγές στον αριθμό ορισμένων κυττάρων του αίματος των οποίων η ανεπάρκεια οδηγεί σε αναιμία ή επηρεάζει την ικανότητα πήξης του αίματος. Ο κίνδυνος αιμορραγίας μπορεί να είναι υψηλότερος εάν παίρνετε βαρφαρίνη ή ακενοκουμαρόλη, φάρμακα που αραιώνουν το αίμα για την πρόληψη θρόμβων αίματος. Ενημερώστε το γιατρό σας εάν εμφανίσετε αιμορραγία ενώ παίρνετε το Sutent.
- Εάν έχετε καρδιακά προβλήματα. Το Sutent μπορεί να προκαλέσει καρδιακά προβλήματα. Ενημερώστε το γιατρό σας εάν αισθάνεστε πολύ κουρασμένοι, έχετε δύσπνοια ή πρησμένα πόδια και αστραγάλους.
- Εάν αντιμετωπίσετε μη φυσιολογικές αλλαγές στον καρδιακό ρυθμό. Το Sutent μπορεί να προκαλέσει αλλαγές στον καρδιακό ρυθμό. Ενώ λαμβάνετε θεραπεία με Sutent, ο γιατρός σας μπορεί να κάνει ηλεκτροκαρδιογράφημα για να εκτιμήσει την έκταση αυτών των αλλαγών. Ενημερώστε το γιατρό σας εάν αισθάνεστε ζάλη, λιποθυμία ή έχετε μη φυσιολογικούς καρδιακούς παλμούς ενώ παίρνετε το Sutent.
- Εάν είχατε πρόσφατα προβλήματα με θρόμβους αίματος στις φλέβες και / ή τις αρτηρίες σας (τύποι αιμοφόρων αγγείων), συμπεριλαμβανομένου εγκεφαλικού επεισοδίου, καρδιακής προσβολής, εμβολής ή θρόμβωσης. Επικοινωνήστε αμέσως με το γιατρό σας εάν εμφανίσετε συμπτώματα όπως σφίξιμο στο στήθος ή πόνο, πόνο στα χέρια, την πλάτη, το λαιμό ή το σαγόνι, δύσπνοια, μούδιασμα ή αδυναμία στη μία πλευρά του σώματος, τρεμάμενο περπάτημα, πόνος κατά τη διάρκεια της θεραπείας με κεφαλαλγία Sutent ή ζάλη.
- Εάν έχετε προβλήματα με τον θυρεοειδή. Το Sutent μπορεί να προκαλέσει προβλήματα στον θυρεοειδή. Ενημερώστε το γιατρό σας εάν κουραστείτε πιο εύκολα ενώ παίρνετε το Sutent, γενικά αισθάνεστε πιο κρύο από άλλα άτομα ή εάν η φωνή σας πέσει. Η λειτουργία του θυρεοειδούς πρέπει να ελέγχεται πριν πάρετε το Sutent και τακτικά ενώ παίρνετε το φάρμακο. Εάν ο θυρεοειδής δεν παράγει αρκετή ορμόνη θυρεοειδούς, μπορεί να χρειαστεί να πάρετε μια ορμόνη αντικατάστασης θυρεοειδούς.
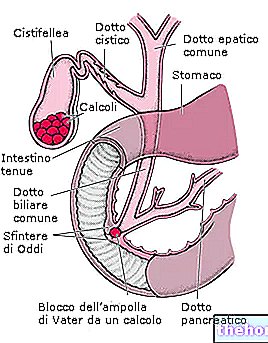
- Εάν έχετε ή είχατε προβλήματα με το πάγκρεας ή τη χοληδόχο κύστη σας. Ενημερώστε το γιατρό σας εάν εμφανίσετε οποιοδήποτε από τα ακόλουθα σημεία και συμπτώματα: πόνος στο στομάχι (άνω κοιλιά), ναυτία, έμετος και πυρετός. Αυτά μπορεί να προκληθούν από φλεγμονή του παγκρέατος ή της χοληδόχου κύστης.
- Εάν έχετε ή είχατε ποτέ ηπατικά προβλήματα. Ενημερώστε το γιατρό σας εάν εμφανίσετε οποιοδήποτε από τα ακόλουθα σημεία και συμπτώματα ηπατικών προβλημάτων κατά τη διάρκεια της θεραπείας με Sutent: κνησμό, κιτρίνισμα του δέρματος ή των ματιών, σκούρα ούρα και πόνο ή ενόχληση στην άνω δεξιά περιοχή του στομάχου. Ο γιατρός σας για τον έλεγχο της ηπατικής λειτουργίας πριν και κατά τη διάρκεια της θεραπείας με Sutent, και όπως είναι κλινικά κατάλληλο.
- Εάν έχετε ή είχατε νεφρικά προβλήματα. Ο γιατρός θα παρακολουθεί τη λειτουργία των νεφρών.
- Εάν πρόκειται να υποβληθείτε σε χειρουργική επέμβαση ή είχατε μια επέμβαση πρόσφατα. Το Sutent μπορεί να επηρεάσει τον τρόπο επούλωσης των πληγών σας. Γενικά εάν πρόκειται να υποβληθείτε σε επέμβαση θα πρέπει να σταματήσετε να χρησιμοποιείτε το Sutent. Ο γιατρός σας θα αποφασίσει πότε θα ξεκινήσει ξανά τη θεραπεία με Sutent.
- Συνιστάται να κάνετε έναν οδοντιατρικό έλεγχο πριν ξεκινήσετε τη θεραπεία με το Sutent.
- εάν έχετε ή είχατε πόνο στο στόμα, τα δόντια και / ή τη γνάθο, πρήξιμο ή πληγές στο στόμα, μούδιασμα ή αίσθημα βάρους στη γνάθο ή χαλάρωση των δοντιών, ενημερώστε αμέσως τον γιατρό και τον οδοντίατρό σας.
- εάν υποβάλλεστε σε επεμβατική οδοντιατρική θεραπεία ή οδοντιατρική χειρουργική επέμβαση, ενημερώστε το γιατρό σας ότι λαμβάνετε θεραπεία με Sutent, ιδιαίτερα εάν λαμβάνετε επίσης ενδοφλέβια διφωσφονικά ή τα έχετε λάβει προηγουμένως.Τα διφωσφονικά είναι φάρμακα που χρησιμοποιούνται για την πρόληψη των επιπλοκών των οστών που μπορεί να έχουν συνταγογραφηθεί για άλλο ιατρικό πρόβλημα.
- Εάν έχετε ή είχατε ποτέ διαταραχές του δέρματος και του υποδόριου ιστού. Κατά τη διάρκεια της θεραπείας με αυτό το φάρμακο μπορεί να εμφανιστεί «γαγγραινώδες πυόδερμα» (επώδυνο έλκος του δέρματος) ή «νεκρωτική απονευρωσίτιδα» (μια ταχέως εξαπλωμένη «λοίμωξη δέρματος / μαλακών ιστών» που μπορεί να είναι θανατηφόρα). Διακοπή της θεραπείας. Σοβαρές δερματικές αντιδράσεις (Stevens-Johnson σύνδρομο, τοξική επιδερμική νεκρόλυση, πολύμορφο ερύθημα) έχουν αναφερθεί με τη χρήση του sunitinib, αρχικά εμφανιζόμενα στον κορμό ως κοκκινωπές κηλίδες σε σχήμα στόχου ή κυκλικά μπαλώματα, συχνά με φουσκάλες στο κέντρο. Η αντίδραση μπορεί να εξελιχθεί σε εκτεταμένες φουσκάλες ή ξεφλούδισμα του δέρματος και μπορεί να αποβεί μοιραία. Εάν εμφανίσετε εξάνθημα ή οποιοδήποτε από αυτά τα συμπτώματα του δέρματος, συμβουλευτείτε αμέσως γιατρό.
- Εάν έχετε ή είχατε επιληπτικές κρίσεις. Ενημερώστε το γιατρό σας το συντομότερο δυνατό εάν έχετε υψηλή αρτηριακή πίεση, πονοκέφαλο, απώλεια όρασης.
- Εάν έχετε διαβήτη. Τα επίπεδα σακχάρου στο αίμα πρέπει να ελέγχονται τακτικά σε διαβητικούς ασθενείς για να διαπιστωθεί εάν πρέπει να αλλάξει η δοσολογία των φαρμάκων για τον διαβήτη προκειμένου να ελαχιστοποιηθεί ο κίνδυνος χαμηλού σακχάρου στο αίμα.
Παιδιά και έφηβοι
Το Sutent δεν ενδείκνυται για ασθενείς ηλικίας κάτω των 18 ετών. Το Sutent δεν έχει μελετηθεί σε παιδιά και εφήβους.
Αλληλεπιδράσεις Ποια φάρμακα ή τρόφιμα μπορούν να τροποποιήσουν την επίδραση του Sutent
Ενημερώστε τον γιατρό ή τον φαρμακοποιό σας εάν παίρνετε, έχετε πάρει πρόσφατα ή μπορεί να πάρετε άλλα φάρμακα, συμπεριλαμβανομένων αυτών που αγοράστηκαν χωρίς ιατρική συνταγή και εκείνων που δεν έχουν συνταγή.
Ορισμένα φάρμακα μπορούν να αλλάξουν τα επίπεδα του Sutent στο σώμα. Θα πρέπει να ενημερώσετε το γιατρό σας εάν παίρνετε φάρμακα που περιέχουν τις ακόλουθες δραστικές ουσίες:
- κετοκοναζόλη, ιτρακοναζόλη - χρησιμοποιείται για τη θεραπεία μυκητιασικών λοιμώξεων
- ερυθρομυκίνη, κλαριθρομυκίνη, ριφαμπικίνη - χρησιμοποιούνται για τη θεραπεία λοιμώξεων
- ριτοναβίρη - χρησιμοποιείται για τη θεραπεία του AIDS
- δεξαμεθαζόνη - ένα κορτικοστεροειδές που χρησιμοποιείται για διάφορες καταστάσεις
- φαινυτοΐνη, καρβαμαζεπίνη, φαινοβαρβιτάλη - χρησιμοποιούνται για τη θεραπεία της επιληψίας και άλλων νευρολογικών καταστάσεων
- φυτικά σκευάσματα που περιέχουν βαλσαμόχορτο (Hypericum perforatum) - χρησιμοποιούνται για τη θεραπεία της κατάθλιψης και του άγχους
Sutent με φαγητό και ποτό
Κατά τη διάρκεια της θεραπείας με Sutent πρέπει να αποφεύγεται η πρόσληψη χυμού γκρέιπφρουτ.
Προειδοποιήσεις Είναι σημαντικό να γνωρίζετε ότι:
Εγκυμοσύνη και θηλασμός
Εάν είστε έγκυος ή υποψιάζεστε ότι είστε έγκυος, ενημερώστε το γιατρό σας.
Το Sutent δεν πρέπει να χρησιμοποιείται κατά τη διάρκεια της εγκυμοσύνης, εκτός εάν είναι απολύτως απαραίτητο. Ο γιατρός σας θα συζητήσει μαζί σας τους πιθανούς κινδύνους της θεραπείας με Sutent κατά τη διάρκεια της εγκυμοσύνης.
Εάν είναι δυνατή η εγκυμοσύνη, πρέπει να χρησιμοποιείτε μια αξιόπιστη μέθοδο αντισύλληψης ενώ λαμβάνετε θεραπεία με Sutent.
Εάν θηλάζετε, ενημερώστε το γιατρό σας. Δεν πρέπει να θηλάζετε ενώ λαμβάνετε θεραπεία με Sutent.
Οδήγηση και χειρισμός μηχανών
Εάν αισθάνεστε ζάλη ή ασυνήθιστα κουρασμένος, προσέξτε ιδιαίτερα όταν οδηγείτε ή χειρίζεστε μηχανές.
Δόση, μέθοδος και χρόνος χορήγησης Πώς να χρησιμοποιήσετε το Sutent: Δοσολογία
Πάντοτε να παίρνετε αυτό το φάρμακο σύμφωνα με τις οδηγίες του γιατρού σας.
Εάν έχετε αμφιβολίες, συμβουλευτείτε το γιατρό σας. Ο γιατρός σας θα σας συνταγογραφήσει τη σωστή δόση, με βάση τον τύπο του καρκίνου που πρέπει να αντιμετωπίσετε. Εάν λαμβάνετε θεραπεία για GIST ή MRCC, η συνήθης δόση είναι 50 mg μία φορά ημερησίως για λήψη για 28 ημέρες (4 εβδομάδες), ακολουθούμενη από 14 ημέρες (2 εβδομάδες) ανάπαυσης (χωρίς φαρμακευτική αγωγή), σε κύκλους 6 εβδομάδων. Εάν λαμβάνετε θεραπεία για pNET, η συνήθης δόση είναι 37,5 mg μία φορά την ημέρα, χωρίς περίοδο ανάπαυσης. Ο γιατρός σας θα καθορίσει τη δόση που χρειάζεστε και πότε θα σταματήσετε τη θεραπεία με Sutent. Το Sutent μπορεί να ληφθεί με ή χωρίς φαγητό.
Υπερδοσολογία Τι πρέπει να κάνετε εάν έχετε πάρει πάρα πολύ Sutent
Εάν πάρετε μεγαλύτερη δόση Sutent από την κανονική
Εάν έχετε πάρει κατά λάθος πάρα πολλές κάψουλες, μιλήστε αμέσως με το γιατρό σας. Μπορεί να απαιτείται ιατρική φροντίδα
Εάν ξεχάσετε να πάρετε το Sutent
Μην πάρετε διπλή δόση για να αναπληρώσετε τη δόση που ξεχάσατε.
Παρενέργειες Ποιες είναι οι παρενέργειες του Sutent
Όπως όλα τα φάρμακα, αυτό το φάρμακο μπορεί να προκαλέσει ανεπιθύμητες ενέργειες, αν και δεν παρουσιάζονται σε όλους τους ανθρώπους.
Επικοινωνήστε αμέσως με το γιατρό σας εάν εμφανίσετε κάποια από αυτές τις σοβαρές ανεπιθύμητες ενέργειες (δείτε επίσης Τι πρέπει να γνωρίζετε προτού πάρετε το Sutent):
Καρδιακά προβλήματα. Ενημερώστε το γιατρό σας εάν αισθάνεστε πολύ κουρασμένοι, έχετε δύσπνοια ή πρησμένα πόδια και αστραγάλους. Αυτά θα μπορούσαν να είναι συμπτώματα καρδιακών προβλημάτων όπως καρδιακή ανεπάρκεια και προβλήματα καρδιακών μυών (καρδιομυοπάθεια).
Προβλήματα πνευμόνων ή αναπνοής. Ενημερώστε το γιατρό σας εάν εμφανίσετε βήχα, πόνο στο στήθος, ξαφνική εμφάνιση δύσπνοιας ή βήχα αίματος. Αυτά θα μπορούσαν να είναι συμπτώματα πνευμονικής εμβολής που συμβαίνει όταν οι θρόμβοι αίματος ταξιδεύουν στους πνεύμονες.
Νεφρικά προβλήματα. Ενημερώστε το γιατρό σας εάν εμφανίσετε μια «αλλοιωμένη συχνότητα ή απουσία ούρησης, η οποία θα μπορούσε να είναι συμπτώματα» νεφρικής ανεπάρκειας.
Αιμορραγία. Ενημερώστε το γιατρό σας αμέσως εάν εμφανίσετε οποιοδήποτε από τα ακόλουθα συμπτώματα ή σοβαρό πρόβλημα αιμορραγίας κατά τη λήψη του Sutent: πρησμένο, επώδυνο στομάχι (κοιλιά). έμετος με αίμα. σκούρα, κολλώδη κόπρανα. πονοκέφαλος ή αλλαγές στην ψυχική κατάσταση, βήχας αίματος ή πτυέλων με αίμα από τους πνεύμονες ή τους αεραγωγούς.
Καταστροφή του όγκου που προκαλεί διάτρηση του εντέρου. Ενημερώστε το γιατρό σας εάν έχετε έντονο πόνο στο έντερο, πυρετό, ναυτία, έμετο, αίμα στα κόπρανα ή αλλαγές στις συνήθειες του εντέρου.
Άλλες ανεπιθύμητες ενέργειες που μπορεί να εμφανιστούν με το Sutent είναι:
Πολύ συχνές ανεπιθύμητες ενέργειες (μπορεί να επηρεάσουν περισσότερα από 1 στα 10 άτομα)
- Μείωση του αριθμού των αιμοπεταλίων, των ερυθρών αιμοσφαιρίων και / ή των λευκών αιμοσφαιρίων (π.χ. ουδετερόφιλα).
- Δυσκολία στην αναπνοή
- Υψηλή πίεση του αίματος.
- Υπερβολική κούραση, απώλεια δύναμης.
- Οίδημα που προκαλείται από υγρό κάτω από το δέρμα και γύρω από τα μάτια, βαθύ αλλεργικό εξάνθημα.
- Στοματικός πόνος / ερεθισμός, πόνος / φλεγμονή / ξηροστομία, διαταραχές της γεύσης, στομαχικές διαταραχές, ναυτία, έμετος, διάρροια, δυσκοιλιότητα, κοιλιακό άλγος / πρήξιμο, απώλεια / μείωση της όρεξης.
- Μειωμένη δραστηριότητα του θυρεοειδούς αδένα (υποθυρεοειδισμός).
- Ζάλη
- Πονοκέφαλο.
- Ματωμένη μύτη.
- Πόνος στην πλάτη, πόνος στις αρθρώσεις.
- Πόνος στα χέρια και τα πόδια.
- Κιτρίνισμα του δέρματος / αποχρωματισμός του δέρματος, υπερβολική χρώση του δέρματος, αποχρωματισμός των μαλλιών, εξάνθημα στις παλάμες και τα πέλματα των ποδιών, εξάνθημα, ξηροδερμία.
- Βήχας.
- Πυρετός.
- Δυσκολία στον ύπνο.
Συχνές ανεπιθύμητες ενέργειες (μπορεί να επηρεάσουν 1 έως 10 στα 100 άτομα)
- Σχηματισμός θρόμβων στα αιμοφόρα αγγεία.
- Ανεπαρκής παροχή αίματος στον καρδιακό μυ, λόγω απόφραξης ή συστολής των στεφανιαίων αρτηριών.
- Πόνος στο στήθος.
- Μειωμένη ποσότητα αίματος που αντλείται από την καρδιά.
- Κατακράτηση υγρών και γύρω από τους πνεύμονες.
- Λοιμώξεις.
- Μειωμένο επίπεδο σακχάρου στο αίμα. Εάν εμφανίσετε σημεία και συμπτώματα χαμηλού σακχάρου στο αίμα: Ενημερώστε το γιατρό σας το συντομότερο δυνατό εάν εμφανίσετε κόπωση, αίσθημα παλμών, εφίδρωση, πείνα και απώλεια συνείδησης.
- Απώλεια πρωτεΐνης στα ούρα, η οποία μερικές φορές οδηγεί σε οίδημα.
- Σύνδρομο γρίπης.
- Μη φυσιολογικές εξετάσεις αίματος, συμπεριλαμβανομένων των επιπέδων των ηπατικών ενζύμων και του παγκρέατος.
- Υψηλά επίπεδα ουρικού οξέος στο αίμα.
- Αιμορροΐδες, πόνος στο ορθό, αιμορραγία των ούλων, δυσκολία στην κατάποση ή αδυναμία κατάποσης.
- Κάψιμο ή οδυνηρή αίσθηση στη γλώσσα, φλεγμονή του βλεννογόνου της πεπτικής οδού, περίσσεια αερίων στο στομάχι ή τα έντερα.
- Απώλεια βάρους.
- Μυοσκελετικός πόνος (πόνος στους μυς και τα οστά), μυϊκή αδυναμία, μυϊκή κόπωση, μυϊκός πόνος, μυϊκοί σπασμοί.
- Ρινική ξηρότητα, ρινική συμφόρηση.
- Υπερβολικό σκίσιμο.
- Αλλαγές στην ευαισθησία του δέρματος, ξηροδερμία, κνησμό, ξεφλούδισμα και φλεγμονή του δέρματος, φουσκάλες, ακμή, αποχρωματισμό των νυχιών, τριχόπτωση.
- Μη φυσιολογικές αισθήσεις στα άκρα.
- Υπερβολική μείωση / αύξηση της ευαισθησίας, ειδικά στην αφή.
- Κάψιμο στο στομάχι.
- Αφυδάτωση.
- Ερυθρότητα προσώπου.
- Αλλαγή στο χρώμα των ούρων.
- Κατάθλιψη.
- Κρυάδα.
Όχι συχνές ανεπιθύμητες ενέργειες (μπορεί να επηρεάσουν 1 έως 10 στα 1.000 άτομα)
- Λοιμώξεις μαλακών ιστών, συμπεριλαμβανομένης της περιοχής των γεννητικών οργάνων, δυνητικά απειλητικές για τη ζωή.Επικοινωνήστε αμέσως με το γιατρό σας εάν εμφανίσετε συμπτώματα λοίμωξης γύρω από μια πληγή του δέρματος, όπως πυρετό, πόνο, ερυθρότητα, πρήξιμο ή παροχέτευση πύου ή αίματος.
- Εγκεφαλικό.
- Καρδιακή προσβολή που προκαλείται από διακοπή ή μείωση της παροχής αίματος στην καρδιά.
- Αλλαγές στην ηλεκτρική δραστηριότητα της καρδιάς ή αλλοιωμένος καρδιακός ρυθμός.
- Υγρό γύρω από την καρδιά (περικαρδιακή συλλογή).
- Ηπατική ανεπάρκεια.
- Πόνος στο στομάχι (κοιλιά) που προκαλείται από «φλεγμονή του παγκρέατος.
- Καταστροφή του όγκου προκαλώντας διάτρηση του εντέρου.
- Φλεγμονή (πρήξιμο και ερυθρότητα) της χοληδόχου κύστης με ή χωρίς σχετικούς λίθους.
- Μη φυσιολογικό κανάλι επικοινωνίας μεταξύ δύο κοιλοτήτων του σώματος ή με το δέρμα.
- Πόνος στο στόμα, δόντια και / ή γνάθο, πρήξιμο ή ερεθισμός στο στόμα, μούδιασμα ή αίσθημα βάρους στη γνάθο ή χαλάρωση των δοντιών. Αυτά μπορεί να είναι τα σημάδια και τα συμπτώματα τραυματισμού οστού της γνάθου (οστεονέκρωση). Ενημερώστε αμέσως το γιατρό και τον οδοντίατρό σας εάν εμφανίσετε κάποιο από αυτά τα σημεία και συμπτώματα.
- Η υπερβολική παραγωγή θυρεοειδικών ορμονών με αποτέλεσμα αυξημένο μεταβολισμό. Προβλήματα με την επούλωση πληγών μετά από χειρουργική επέμβαση.
- Αύξηση μυϊκού ενζύμου στο αίμα (φωσφοκινάση κρεατίνης).
- Ακατάλληλη και υπερβολική αντίδραση σε αλλεργιογόνα.
Σπάνιες ανεπιθύμητες ενέργειες (μπορεί να επηρεάσουν 1 έως 10 στα 10.000 άτομα)
- Σοβαρές αντιδράσεις του δέρματος ή / και των βλεννογόνων (σύνδρομο Stevens-Johnson, τοξική επιδερμική νεκρόλυση, πολύμορφο ερύθημα).
- Σύνδρομο λύσης όγκου (TLS) - Το TLS περιλαμβάνει ένα σύνολο μεταβολικών επιπλοκών που μπορεί να προκύψουν κατά τη θεραπεία του καρκίνου. Προκαλούνται από τα προϊόντα διάσπασης των προσβεβλημένων καρκινικών κυττάρων και μπορεί να περιλαμβάνουν: ναυτία, δύσπνοια, ακανόνιστο καρδιακό παλμό, μυϊκές κράμπες, σπασμούς, θολό ούρα και κόπωση που σχετίζονται με μη φυσιολογικά αποτελέσματα εργαστηριακών εξετάσεων (υψηλά επίπεδα καλίου, ουρικού οξέος και φωσφορικού οξέος και χαμηλά επίπεδα ασβεστίου στο αίμα) που μπορεί να οδηγήσουν σε αλλαγές στη λειτουργία των νεφρών και οξεία νεφρική ανεπάρκεια.
- Μη φυσιολογική διάσπαση των μυών που μπορεί να προκαλέσει νεφρικά προβλήματα (ραβδομυόλυση).
- Διαταραχή της λειτουργίας του εγκεφάλου που μπορεί να οδηγήσει σε ποικίλα συμπτώματα, όπως πονοκέφαλο, σύγχυση, επιληπτικές κρίσεις και απώλεια όρασης (σύνδρομο οπίσθιας αναστρέψιμης λευκοεγκεφαλοπάθειας).
- Επώδυνη εξέλκωση του δέρματος (γαγγραινώδες πυόδερμα).
- Φλεγμονή του ήπατος (ηπατίτιδα).
- Φλεγμονή του θυρεοειδούς αδένα.
Αναφορά παρενεργειών
Εάν παρατηρήσετε κάποια ανεπιθύμητη ενέργεια, ενημερώστε το γιατρό σας. Αυτό περιλαμβάνει τυχόν ανεπιθύμητες ενέργειες που δεν αναφέρονται στο παρόν φύλλο οδηγιών. Μπορείτε επίσης να αναφέρετε ανεπιθύμητες ενέργειες απευθείας μέσω του εθνικού συστήματος αναφοράς που παρατίθεται στο Παράρτημα V. Αναφέροντας ανεπιθύμητες ενέργειες μπορείτε να βοηθήσετε στην παροχή περισσότερων πληροφοριών σχετικά με την ασφάλεια αυτού του φαρμάκου.
Λήξη και διατήρηση
- Κρατήστε αυτό το φάρμακο μακριά από τα μάτια και την πρόσβαση των παιδιών.
- Μη χρησιμοποιείτε αυτό το φάρμακο μετά την ημερομηνία λήξης που αναφέρεται στο κουτί και στην ετικέτα μετά το "ΛΗΞΗ". Η ημερομηνία λήξης αναφέρεται στην τελευταία ημέρα του μήνα.
- Αυτό το φαρμακευτικό προϊόν δεν απαιτεί ειδικές συνθήκες φύλαξης.
- Μην χρησιμοποιείτε αυτό το φάρμακο εάν παρατηρήσετε ότι η συσκευασία είναι κατεστραμμένη ή εμφανίζει σημάδια παραποίησης.
Μην πετάτε φάρμακα μέσω λυμάτων ή οικιακών απορριμμάτων. Ρωτήστε τον φαρμακοποιό σας πώς να πετάξετε φάρμακα που δεν χρησιμοποιείτε πια. Αυτό θα βοηθήσει στην προστασία του περιβάλλοντος.
Τι περιέχει το Sutent
Sutent σκληρά καψάκια 12,5 mg
Το δραστικό συστατικό είναι η σουνιτινίμπη. Κάθε κάψουλα περιέχει malate sunitinib ισοδύναμο με 12,5 mg sunitinib.
Τα άλλα συστατικά είναι:
- Περιεχόμενα κάψουλας: μαννιτόλη (Ε421), νατριούχος κροσκαρμελλόζη, ποβιδόνη (Κ-25) και στεατικό μαγνήσιο.
- Κέλυφος κάψουλας: ζελατίνη, κόκκινο οξείδιο του σιδήρου (Ε172) και διοξείδιο του τιτανίου (Ε171).
- Μελάνι: shellac, προπυλενογλυκόλη, υδροξείδιο του νατρίου, ποβιδόνη και διοξείδιο του τιτανίου (Ε171).
Sutent σκληρά καψάκια 25 mg
Το δραστικό συστατικό είναι η σουνιτινίμπη. Κάθε κάψουλα περιέχει malate sunitinib ισοδύναμο με 25 mg sunitinib.
Τα άλλα συστατικά είναι:
- Περιεχόμενα κάψουλας: μαννιτόλη (Ε421), νατριούχος κροσκαρμελλόζη, ποβιδόνη (Κ-25) και στεατικό μαγνήσιο.
- Κέλυφος κάψουλας: ζελατίνη, διοξείδιο του τιτανίου (Ε171), κίτρινο οξείδιο του σιδήρου (Ε172), κόκκινο οξείδιο του σιδήρου (Ε172), μαύρο οξείδιο του σιδήρου (Ε172).
- Μελάνι: shellac, προπυλενογλυκόλη, υδροξείδιο του νατρίου, ποβιδόνη και διοξείδιο του τιτανίου (E171)
Sutent 37,5 mg σκληρά καψάκια
Το δραστικό συστατικό είναι η σουνιτινίμπη. Κάθε κάψουλα περιέχει malate sunitinib ισοδύναμο με 37,5 mg sunitinib.
Τα άλλα συστατικά είναι:
- Περιεχόμενα κάψουλας: μαννιτόλη (Ε421), νατριούχος κροσκαρμελλόζη, ποβιδόνη (Κ-25) και στεατικό μαγνήσιο.
- Κέλυφος κάψουλας: ζελατίνη, διοξείδιο του τιτανίου (Ε171), κίτρινο οξείδιο του σιδήρου (Ε172).
- Μελάνι: shellac, προπυλενογλυκόλη, υδροξείδιο του καλίου, μαύρο οξείδιο του σιδήρου (E172).
Sutent σκληρά καψάκια 50 mg
Το δραστικό συστατικό είναι η σουνιτινίμπη. Κάθε κάψουλα περιέχει malate sunitinib ισοδύναμο με 50 mg sunitinib.
Τα άλλα συστατικά είναι:
- Περιεχόμενα κάψουλας: μαννιτόλη (Ε421), νατριούχος κροσκαρμελλόζη, ποβιδόνη (Κ-25) και στεατικό μαγνήσιο.
- Κέλυφος κάψουλας: ζελατίνη, διοξείδιο του τιτανίου (Ε171), κίτρινο οξείδιο του σιδήρου (Ε172), κόκκινο οξείδιο του σιδήρου (Ε172) και μαύρο οξείδιο του σιδήρου (Ε172).
- Μελάνι: shellac, προπυλενογλυκόλη, υδροξείδιο του νατρίου, ποβιδόνη και διοξείδιο του τιτανίου (Ε171).
Περιγραφή της εμφάνισης του Sutent και του περιεχομένου της συσκευασίας
Το Sutent 12,5 mg διατίθεται ως κάψουλες σκληρής ζελατίνης με πορτοκαλί κάλυμμα και σώμα, με "Pfizer" με λευκό μελάνι στο πώμα και "STN 12,5 mg" στο σώμα, που περιέχουν χρωματιστούς κόκκους. Κίτρινο-πορτοκαλί.
Το Sutent 25 mg διατίθεται ως κάψουλες σκληρής ζελατίνης με καπάκι καραμέλας και πορτοκαλί σώμα, με "Pfizer" με λευκό μελάνι στο καπάκι και "STN 25 mg" στο σώμα, που περιέχει χρωματιστούς κόκκους. Κίτρινο-πορτοκαλί.
Το Sutent 37,5 mg διατίθεται ως κάψουλες σκληρής ζελατίνης με κίτρινο κάλυμμα και σώμα, με το "Pfizer" με μαύρο μελάνι στο πώμα και "STN 37,5 mg" στο σώμα, που περιέχει χρωματιστούς κόκκους. Κίτρινο-πορτοκαλί.
Το Sutent 50 mg διατίθεται ως κάψουλες σκληρής ζελατίνης με καπάκι και σώμα με χρώμα καραμέλας, με "Pfizer" με λευκό μελάνι στο καπάκι και "STN 50 mg" στο σώμα, που περιέχουν κίτρινο-πορτοκαλί κόκκους. Διατίθεται σε φιάλες 30 καψουλών και διάτρητες κυψέλες μοναδιαίας δόσης που περιέχουν 28 κάψουλες.
Μπορεί να μην κυκλοφορούν όλες οι συσκευασίες.
Φύλλο οδηγιών χρήσης: AIFA (Ιταλικός Οργανισμός Φαρμάκων). Περιεχόμενο που δημοσιεύτηκε τον Ιανουάριο του 2016. Οι πληροφορίες που υπάρχουν δεν μπορεί να είναι ενημερωμένες.
Για να έχετε πρόσβαση στην πιο ενημερωμένη έκδοση, είναι σκόπιμο να αποκτήσετε πρόσβαση στον ιστότοπο AIFA (Ιταλικός Οργανισμός Φαρμάκων). Αποποίηση ευθυνών και χρήσιμες πληροφορίες.
01.0 ΟΝΟΜΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟDΟΝΤΟΣ
SUTENT 12,5 MG ΣΚΛΗΡΕΣ ΚΑΠΟΥΛΕΣ
02.0 ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
Κάθε κάψουλα περιέχει malate sunitinib, που αντιστοιχεί σε 12,5 mg sunitinib.
Για τον πλήρη κατάλογο των εκδόχων, ανατρέξτε στην ενότητα 6.1.
03.0 ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ
Σκληρή κάψουλα.
Κάψουλες ζελατίνης με πορτοκαλί κάλυμμα και σώμα, σημειωμένες με λευκό μελάνι "Pfizer" στο πώμα, "STN 12,5 mg" στο σώμα και περιέχουν κίτρινο-πορτοκαλί κόκκους.
04.0 ΚΛΙΝΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ
04.1 Θεραπευτικές ενδείξεις
Στρωματικός όγκος του γαστρεντερικού σωλήνα (GIST)
Το SUTENT ενδείκνυται για τη θεραπεία μη ανιχνεύσιμου και / ή μεταστατικού γαστρεντερικού στρωματικού καρκίνου (GIST) σε ενήλικες μετά από αποτυχία της θεραπείας με imatinib λόγω αντοχής ή δυσανεξίας.
Μεταστατικό καρκίνωμα νεφρικών κυττάρων (MRCC)
Το SUTENT ενδείκνυται για τη θεραπεία προχωρημένου / μεταστατικού καρκινώματος νεφρικών κυττάρων (MRCC) σε ενήλικες.
Παγκρεατικοί νευροενδοκρινικοί όγκοι (pNET)
Το SUTENT ενδείκνυται για τη θεραπεία καλώς διαφοροποιημένων, μη ανιχνεύσιμων ή μεταστατικών νευροενδοκρινών όγκων του παγκρέατος (pNETs) σε εξελισσόμενη νόσο σε ενήλικες.
Η εμπειρία με το SUTENT ως φάρμακο πρώτης γραμμής είναι περιορισμένη (βλ. Παράγραφο 5.1).
04.2 Δοσολογία και τρόπος χορήγησης
Η θεραπεία με Sunitinib πρέπει να ξεκινήσει από γιατρό έμπειρο στη χορήγηση αντικαρκινικών παραγόντων.
Δοσολογία
Για το GIST και το MRCC, η συνιστώμενη δόση SUTENT είναι 50 mg που πρέπει να λαμβάνεται από το στόμα μία φορά την ημέρα, για 4 συνεχόμενες εβδομάδες, ακολουθούμενη από 2 εβδομάδες ανάπαυσης (πρόγραμμα 4/2) προκειμένου να πραγματοποιηθεί μια πλήρης πορεία 6 εβδομάδων.
Για το pNET, η συνιστώμενη δόση του SUTENT είναι 37,5 mg που πρέπει να λαμβάνεται από το στόμα μία φορά την ημέρα, χωρίς προγραμματισμένη περίοδο ανάπαυσης.
Ρύθμιση δόσης
Ασφάλεια και ανεκτικότητα
Για το GIST και το MRCC, τροποποιήσεις της δόσης σε προσαυξήσεις των 12,5 mg μπορούν να γίνουν με βάση την ασφάλεια και την ανεκτικότητα του κάθε ασθενούς. Η ημερήσια δόση δεν πρέπει να υπερβαίνει τα 75 mg ούτε να μειώνεται κάτω από τα 25 mg.
Για το pNET, μπορούν να γίνουν τροποποιήσεις της δοσολογίας σε προσαυξήσεις των 12,5 mg με βάση την ασφάλεια και την ανεκτικότητα του κάθε ασθενούς. Η μέγιστη δόση που χορηγήθηκε στη μελέτη pNET φάσης 3 ήταν 50 mg ημερησίως.
Μπορεί να χρειαστεί να ανασταλεί η λήψη ορισμένων δόσεων με βάση την ασφάλεια και την ανεκτικότητα του κάθε ασθενούς.
Αναστολείς / επαγωγείς του CYP3A4
Η συγχορήγηση σουνιτινίμπης με ισχυρούς επαγωγείς του CYP3A4, όπως η ριφαμπικίνη, θα πρέπει να αποφεύγεται (βλέπε παραγράφους 4.4. Και 4.5). Εάν αυτό δεν είναι δυνατό, η δόση της σουνιτινίμπης μπορεί να χρειαστεί να αυξηθεί σε αυξήσεις 12,5 mg (έως 87,5 mg / ημέρα για GIST και MRCC ή 62,5 mg / ημέρα για pNET) με βάση την προσεκτική παρακολούθηση της ανεκτικότητας.
Η συγχορήγηση σουνιτινίμπης με ισχυρούς αναστολείς του CYP3A4, όπως η κετοκοναζόλη, θα πρέπει να αποφεύγεται (βλέπε παραγράφους 4.4 και 4.5). Εάν αυτό δεν είναι δυνατό, η δόση της σουνιτινίμπης μπορεί να χρειαστεί να μειωθεί σε μια ελάχιστη δόση 37,5 mg ημερησίως για GIST και MRCC ή 25 mg ημερησίως για pNET, βάσει προσεκτικής παρακολούθησης της ανεκτικότητας.
Θα πρέπει να εξεταστεί η επιλογή εναλλακτικού ταυτόχρονου φαρμακευτικού προϊόντος χωρίς ή ελάχιστη δυνατότητα να επάγει ή να αναστείλει το CYP3A4.
Ειδικοί πληθυσμοί
Παιδιατρικός πληθυσμός
Η ασφάλεια και η αποτελεσματικότητα του sunitinib σε ασθενείς ηλικίας κάτω των 18 ετών δεν έχουν τεκμηριωθεί.
Δεν υπάρχουν διαθέσιμα δεδομένα.
Δεν υπάρχει ένδειξη για συγκεκριμένη χρήση της σουνιτινίμπης σε παιδιά από τη γέννηση έως την ηλικία των 6 ετών στη θεραπεία μη αναστρέψιμων και / ή μεταστατικών GIST μετά από αποτυχία της θεραπείας με ιματινίμπη λόγω αντοχής ή δυσανεξίας. Δεν υπάρχει ένδειξη για συγκεκριμένη χρήση του sunitinib στον παιδιατρικό πληθυσμό στη θεραπεία του MRCC και στη θεραπεία των καλά διαφοροποιημένων, μη αναστρέψιμων ή μεταστατικών pNETs στην πρόοδο της νόσου.
Η χρήση του sunitinib στον παιδιατρικό πληθυσμό δεν συνιστάται.
Ηλικιωμένοι ασθενείς (≥ 65 ετών)
Περίπου το ένα τρίτο των ασθενών που συμμετείχαν σε κλινικές δοκιμές που έλαβαν sunitinib ήταν ηλικίας 65 ετών και άνω. Δεν παρατηρήθηκαν σημαντικές διαφορές στην ασφάλεια και την αποτελεσματικότητα μεταξύ νεότερων και μεγαλύτερων ατόμων.
Ηπατική δυσλειτουργία
Δεν απαιτείται αρχική προσαρμογή της δοσολογίας όταν το sunitinib χορηγείται σε ασθενείς με ήπια ή μέτρια ηπατική δυσλειτουργία (στάδιο Α και Β Child-Pugh). Η χρήση του sunitinib σε άτομα με σοβαρή ηπατική δυσλειτουργία (στάδιο C-Child-Pugh) δεν έχει μελετηθεί, επομένως η χρήση του σε ασθενείς με ηπατική δυσλειτουργία δεν συνιστάται (βλ. Παράγραφο 5.2).
Νεφρική δυσλειτουργία
Δεν απαιτείται αρχική προσαρμογή της δόσης όταν το sunitinib χορηγείται σε ασθενείς με νεφρική δυσλειτουργία (μέτρια έως σοβαρή) ή νεφρική νόσο τελικού σταδίου (ESRD) που υποβάλλονται σε αιμοκάθαρση. Μεταγενέστερες προσαρμογές της δόσης θα πρέπει να γίνονται με βάση την ασφάλεια και την ανεκτικότητα του κάθε ασθενούς (βλ. Παράγραφο 5.2).
Τρόπος χορήγησης
Το SUTENT προορίζεται για στοματική χορήγηση. Μπορεί να ληφθεί με ή χωρίς φαγητό.
Εάν μια δόση δεν ληφθεί, δεν πρέπει να δοθεί επιπλέον δόση. Ο ασθενής θα πρέπει να πάρει τη συνήθη προβλεπόμενη δόση την επόμενη ημέρα.
04.3 Αντενδείξεις
Υπερευαισθησία στη δραστική ουσία ή σε κάποιο από τα έκδοχα που αναφέρονται στην παράγραφο 6.1.
04.4 Ειδικές προειδοποιήσεις και κατάλληλες προφυλάξεις κατά τη χρήση
Η συγχορήγηση με ισχυρούς επαγωγείς του CYP3A4 θα πρέπει να αποφεύγεται καθώς μπορεί να μειώσει τη συγκέντρωση της sunitinib στο πλάσμα (βλέπε παραγράφους 4.2 και 4.5).
Η συγχορήγηση με ισχυρούς αναστολείς του CYP3A4 θα πρέπει να αποφεύγεται καθώς μπορεί να αυξήσει τη συγκέντρωση της sunitinib στο πλάσμα (βλέπε παραγράφους 4.2 και 4.5).
Διαταραχές του δέρματος και των ιστών
Ο αποχρωματισμός του δέρματος, που μπορεί να οφείλεται στο χρώμα της δραστικής ουσίας (κίτρινο), είναι μια πολύ συχνή ανεπιθύμητη ενέργεια που εμφανίζεται σε περίπου 30% των ασθενών. Οι ασθενείς θα πρέπει να ενημερώνονται ότι κατά τη διάρκεια της θεραπείας με sunitinib μπορεί να αποχρωματίσουν τα μαλλιά ή μπορεί επίσης να εμφανιστεί δέρμα. Άλλες πιθανές δερματολογικές επιδράσεις μπορεί να περιλαμβάνουν ξηρότητα, πάχυνση ή ρωγμή του δέρματος, φουσκάλες ή περιστασιακό εξάνθημα στις παλάμες ή τα πέλματα των ποδιών.
Οι παραπάνω αντιδράσεις δεν ήταν αθροιστικές, ήταν γενικά αναστρέψιμες και συνήθως δεν οδήγησαν σε διακοπή της θεραπείας. Έχουν αναφερθεί περιπτώσεις γάγγραινας πυοδερμίας, γενικά αναστρέψιμων μετά τη διακοπή του φαρμάκου. Έχουν αναφερθεί σοβαρές δερματικές αντιδράσεις, συμπεριλαμβανομένων περιπτώσεων πολύμορφου ερυθήματος ( EM) και περιπτώσεις που αποδίδονται στο σύνδρομο Stevens-Johnson (SJS) και την τοξική επιδερμική νεκρόλυση (NET), μερικές από αυτές θανατηφόρες. Με σημεία ή συμπτώματα SJS, NET ή EM (π.χ. δερματικό εξάνθημα συχνά με φουσκάλες ή βλεννογονικές βλάβες) θεραπεία με Εάν η διάγνωση του SJS ή του NET επιβεβαιωθεί, η θεραπεία δεν πρέπει να επαναληφθεί. Σε ορισμένες περιπτώσεις ύποπτου ΗΜ, μετά την επίλυση της αντίδρασης οι ασθενείς έχουν επανεισαγωγή της θεραπείας με sunitinib σε χαμηλότερες ανεκτές δόσεις. μερικοί από αυτούς τους ασθενείς έλαβαν επίσης ταυτόχρονη θεραπεία με κορτικοστεροειδή ή αντισηπτικά ταμίνες.
Αιμορραγία και αιμορραγία που προκαλούνται από όγκους
Αιμορραγικά επεισόδια, ορισμένα με θανατηφόρο αποτέλεσμα, συμπεριλαμβανομένων των γαστρεντερικών, αναπνευστικών, ούρων και εγκεφαλικών αιμορραγιών έχουν αναφερθεί από την εμπειρία μετά την κυκλοφορία.
Τα επεισόδια αιμορραγίας εμφανίστηκαν στο 18% των ασθενών που έλαβαν sunitinib σε σύγκριση με το 17% των ασθενών στην ομάδα του εικονικού φαρμάκου σε μια μελέτη φάσης 3. Οι ασθενείς με MRCC σε sunitinib που δεν είχαν λάβει προηγουμένως θεραπεία με sunitinib ανέφεραν αιμορραγία στο 39% των περιπτώσεων σε σύγκριση με το 11% ασθενών που έλαβαν θεραπεία με IFN-α. Δεκαεπτά (4,5%) ασθενείς σε σουνιτινίμπη σε σύγκριση με 5 (1,7%) ασθενείς σε IFN-α εμφάνισαν επεισόδια αιμορραγίας Βαθμού 3 ή υψηλότερα. Το 26 % των ασθενών που έλαβαν sunitinib για ανθεκτικό στην κυτταροκίνη MRCC ανέφεραν αιμορραγικά επεισόδια. Εκδηλώσεις αιμορραγίας, εξαιρουμένης της επιστάξης, εμφανίστηκαν στο 21,7% των ασθενών που έλαβαν σουνιτινίμπη σε σύγκριση με το 9,85% των ασθενών στην ομάδα του εικονικού φαρμάκου στη Φάση 3 της μελέτης pNET. Η συνηθισμένη αξιολόγηση αυτού του γεγονότος θα πρέπει να περιλαμβάνει πλήρη εξέταση αίματος και φυσική εξέταση.
Η επίσταξη ήταν η πιο συνηθισμένη ανεπιθύμητη αιμορραγική αντίδραση, που είχε αναφερθεί σε περίπου τους μισούς ασθενείς με συμπαγείς όγκους που ανέφεραν αιμορραγικά επεισόδια.Μερικά από αυτά τα επεισόδια επίσταξης ήταν σοβαρά αλλά πολύ σπάνια θανατηφόρα.
Έχουν αναφερθεί περιστατικά αιμορραγίας όγκου, που μερικές φορές σχετίζονται με νέκρωση όγκου. μερικά από αυτά τα αιμορραγικά γεγονότα ήταν θανατηφόρα.
Σε κλινικές δοκιμές, "αιμορραγία όγκου εμφανίστηκε σε περίπου 2% των ασθενών με GIST. Αυτά τα συμβάντα μπορεί να συμβούν ξαφνικά και, στην περίπτωση καρκίνων του πνεύμονα, μπορεί να εμφανιστούν με τη μορφή" σοβαρής και απειλητικής για τη ζωή αιμόπτυσης ή ως πνευμονική αιμορραγία.. Περιπτώσεις πνευμονικής αιμορραγίας, μερικές με θανατηφόρο αποτέλεσμα, έχουν παρατηρηθεί σε κλινικές δοκιμές και έχουν επίσης αναφερθεί μετά την κυκλοφορία σε ασθενείς που έλαβαν sunitinib για MRCC, GIST και καρκίνο του πνεύμονα. Το SUTENT δεν έχει εγκριθεί για χρήση σε ασθενείς με καρκίνο του πνεύμονα.
Ασθενείς που λαμβάνουν ταυτόχρονη θεραπεία με αντιπηκτικά (π.βαρφαρίνη, ακενοκουμαρόλη) μπορεί να παρακολουθείται περιοδικά με πλήρη εξέταση αίματος (αιμοπετάλια), παράγοντες πήξης (PT / INR) και φυσική εξέταση.
Γαστρεντερικές διαταραχές
Διάρροια, ναυτία / έμετος, κοιλιακό άλγος, δυσπεψία και στοματίτιδα / πόνος στο στόμα ήταν οι πιο συχνά αναφερόμενες γαστρεντερικές ανεπιθύμητες ενέργειες. Έχουν επίσης αναφερθεί περιπτώσεις οισοφαγίτιδας (βλ. Παράγραφο 4.8).
Η υποστηρικτική φροντίδα για τις γαστρεντερικές ανεπιθύμητες ενέργειες που απαιτούν θεραπεία μπορεί να περιλαμβάνει φάρμακα με αντιεμετικές, αντιδιαρροϊκές ή αντιόξινες ιδιότητες.
Σοβαρές, μερικές φορές θανατηφόρες, γαστρεντερικές επιπλοκές, συμπεριλαμβανομένης της γαστρεντερικής διάτρησης, έχουν εμφανιστεί σε ασθενείς με ενδοκοιλιακή κακοήθεια που έλαβαν θεραπεία με sunitinib. Στη φάση 3 της μελέτης GIST, θανατηφόρα γαστρεντερική αιμορραγία εμφανίστηκε στο 0,98% των ασθενών που έλαβαν εικονικό φάρμακο.
Υπέρταση
Η υπέρταση ήταν μια πολύ συχνή ανεπιθύμητη ενέργεια που αναφέρθηκε σε κλινικές μελέτες. Η δόση του sunitinib μειώθηκε ή η χορήγησή του αναστέλλεται προσωρινά σε περίπου 2,7% των ασθενών στους οποίους εμφανίστηκε υπέρταση. Σε κανέναν από αυτούς τους ασθενείς το sunitinib δεν διακόπηκε οριστικά. Σοβαρή υπέρταση (> 200 mmHg συστολική ή διαστολική 110 mmHg) εμφανίστηκε στο 4,7% των ασθενών με συμπαγείς όγκους. Σε MRCC και ασθενείς που δεν είχαν λάβει προηγούμενη θεραπεία, αναφέρθηκαν περιπτώσεις υπέρτασης σε 33, 9% των ασθενών σε sunitinib σε σύγκριση με το 3,6% των ασθενών με IFN-α. Επεισόδια σοβαρή υπέρταση εμφανίστηκε στο 12% των ασθενών που δεν είχαν λάβει προηγουμένως θεραπεία στην ομάδα sunitinib και σε λιγότερο από 1% αυτών της ομάδας IFN-α. Στη μελέτη Phase 3 pNET, η υπέρταση αναφέρθηκε στο 26,5% των ασθενών που έλαβαν sunitinib σε σύγκριση με το 4,9% των ασθενών στην ομάδα του εικονικού φαρμάκου. Επεισόδια σοβαρής υπέρτασης εμφανίστηκαν σε ασθενείς με pNET στο 10%. Των ασθενών που έλαβαν sunitinib και 3% Οι ασθενείς πρέπει να υποβάλλονται σε έλεγχο για υπέρταση και να παρακολουθούνται κατάλληλα. Συνιστάται προσωρινή διακοπή της θεραπείας σε ασθενείς με σοβαρή ανεξέλεγκτη υπέρταση με φαρμακευτική αγωγή. Η θεραπεία μπορεί να συνεχιστεί όταν ελέγχεται επαρκώς η υπέρταση.
Αιματολογικές διαταραχές
Παρατηρήθηκε απόλυτη μείωση των αριθμών ουδετερόφιλων Βαθμού 3 και 4 στο 10% και 1,7% των ασθενών που εγγράφηκαν στη μελέτη GIST φάσης 3, αντίστοιχα, και στο 16% και 1,6% των ασθενών που συμπεριλήφθηκαν στη μελέτη. Φάση 3 MRCC και σε 13 % και 2,4% των ασθενών που συμπεριλήφθηκαν στη μελέτη φάσης 3 pNET. Μείωση βαθμού 3 και 4 στον αριθμό αιμοπεταλίων αναφέρθηκε στο 3,7% και 0,4% των ασθενών, αντίστοιχα. ασθενείς που εγγράφηκαν στη μελέτη φάσης 3 GIST, στο 8,2% και 1,1% των ασθενών που συμπεριλήφθηκαν στη μελέτη φάσης 3 MRCC και στο 3,7% και 1,2% των ασθενών που συμπεριλήφθηκαν στη μελέτη φάσης 3 σχετικά με τα pNET.
Τα παραπάνω γεγονότα δεν ήταν αθροιστικά, ήταν γενικά αναστρέψιμα και συνήθως δεν οδήγησαν σε διακοπή της θεραπείας. Κανένα από αυτά τα γεγονότα στις μελέτες φάσης 3 δεν ήταν θανατηφόρο, αλλά σπάνια αιματολογικά συμβάντα έχουν αναφερθεί στη φάση μετά την κυκλοφορία του προϊόντος. συμπεριλαμβανομένης της αιμορραγίας που σχετίζεται με θρομβοπενία και ουδετεροπενικές λοιμώξεις.
Έχει παρατηρηθεί ότι η αναιμία εμφανίζεται τόσο στα πρώιμα όσο και στα τελευταία στάδια της θεραπείας με sunitinib · έχουν αναφερθεί βαθμοί 3 και 4.
Θα πρέπει να πραγματοποιούνται πλήρεις μετρήσεις αίματος στην αρχή κάθε κύκλου θεραπείας σε ασθενείς που λαμβάνουν sunitinib.
Καρδιακές παθολογίες
Καρδιαγγειακά επεισόδια, μερικά από αυτά θανατηφόρα, όπως καρδιακή ανεπάρκεια, καρδιομυοπάθεια, ισχαιμία του μυοκαρδίου και έμφραγμα του μυοκαρδίου, έχουν αναφερθεί σε ασθενείς που έλαβαν θεραπεία με sunitinib. Αυτά τα δεδομένα υποδεικνύουν ότι η sunitinib αυξάνει τον κίνδυνο καρδιομυοπάθειας. Δεν έχουν εντοπιστεί συγκεκριμένοι πρόσθετοι παράγοντες κινδύνου για καρδιομυοπάθεια που προκαλείται από τη σουνιτινίμπη, εκτός από τη συγκεκριμένη επίδραση του φαρμάκου. Οι ασθενείς με σουνιτινίμπη πρέπει να χρησιμοποιούνται με προσοχή σε ασθενείς που διατρέχουν κίνδυνο για αυτά τα συμβάντα ή που έχουν ιστορικό τέτοιων συμβάντων.
Σε κλινικές μελέτες, μειώσεις του κλάσματος εξώθησης της αριστερής κοιλίας (LVEF) ≥ 20% και κάτω από το κατώτερο φυσιολογικό όριο σημειώθηκαν περίπου στο 2% των ασθενών με GIST που έλαβαν θεραπεία με sunitinib, 4% των ασθενών με ανθεκτικό στις κυτοκίνες MRCC που υποβλήθηκαν σε θεραπεία με sunitinib και σε 2 % των ασθενών με GIST που έλαβαν εικονικό φάρμακο. Αυτές οι μειώσεις στο LVEF δεν φαίνεται να είναι προοδευτικές και συχνά βελτιώνονται με τη συνέχιση της θεραπείας. Στη μελέτη που διεξήχθη σε ασθενείς με MRCC και δεν είχαν λάβει προηγούμενη θεραπεία, το 27% των ασθενών που έλαβαν sunitinib και το 15% αυτών που έλαβαν θεραπεία με IFN-α είχαν τιμή LVEF κάτω από το κατώτερο φυσιολογικό όριο. Σε δύο ασθενείς (
Σε ασθενείς με GIST, επεισόδια "καρδιακής ανεπάρκειας", "συμφορητικής καρδιακής ανεπάρκειας" ή "αριστερής κοιλιακής ανεπάρκειας" αναφέρθηκαν στο 1,2% των ασθενών που έλαβαν sunitinib και στο 1% των ασθενών που έλαβαν εικονικό φάρμακο. Στην κεντρική μελέτη στη φάση 3 στο GIST (n = 312), θανατηφόρες καρδιακές αντιδράσεις που σχετίζονται με τη θεραπεία εμφανίστηκαν στο 1% των ασθενών και στα δύο σκέλη της μελέτης (σουνιτινίμπη και βραχίονα εικονικού φαρμάκου). Σε μια μελέτη φάσης 2 σε ασθενείς με ανθεκτικό στην κυτταροκίνη MRCC, το 0,9 % των ασθενών ανέφεραν θανατηφόρο έμφραγμα του μυοκαρδίου που σχετίζεται με τη θεραπεία και σε μελέτη φάσης 3 ασθενών με MRCC και που δεν είχαν λάβει προηγούμενη θεραπεία, 0,6 % των ασθενών στον βραχίονα IFN-α και 0% των ασθενών στον βραχίονα sunitinib ανέφεραν θανατηφόρα καρδιακά συμβάντα. Στη μελέτη Φάσης 3 pNET, ένας ασθενής (1%) που έλαβε sunitinib είχε θανατηφόρα καρδιακή ανεπάρκεια που σχετίζεται με τη θεραπεία. Μια πιθανή συσχέτιση μεταξύ της αναστολής του υποδοχέα κινάσης τυροσίνης (RTK) και της καρδιακής λειτουργίας είναι ασαφής.
Ασθενείς που έχουν αναφέρει καρδιακά συμβάντα, εντός 12 μηνών πριν από τη χορήγηση sunitinib, όπως έμφραγμα του μυοκαρδίου (συμπεριλαμβανομένης της σοβαρής / ασταθούς στηθάγχης), εγχείρηση στεφανιαίας / περιφερικής παράκαμψης, συμπτωματική CHF, εγκεφαλοαγγειακό επεισόδιο ή παροδικό ισχαιμικό επεισόδιο ή πνευμονική εμβολή, εξαιρούνται από κλινικές δοκιμές με sunitinib. Δεν είναι γνωστό εάν ασθενείς με τέτοιες ταυτόχρονες καταστάσεις μπορεί να διατρέχουν αυξημένο κίνδυνο ανάπτυξης δυσλειτουργίας της αριστερής κοιλίας που σχετίζεται με τα ναρκωτικά.
Θα πρέπει να πραγματοποιείται στενή παρακολούθηση για κλινικά σημεία και συμπτώματα συμφορητικής καρδιακής ανεπάρκειας, ιδιαίτερα σε ασθενείς με καρδιακούς παράγοντες κινδύνου και / ή με ιστορικό στεφανιαίας νόσου.
Συνιστάται στους γιατρούς να σταθμίζουν αυτόν τον κίνδυνο με τα πιθανά οφέλη του φαρμάκου. Αυτοί οι ασθενείς θα πρέπει να παρακολουθούνται στενά για κλινικά σημεία και συμπτώματα συμφορητικής καρδιακής ανεπάρκειας κατά τη διάρκεια της θεραπείας με sunitinib. Οι βασικές και περιοδικές εκτιμήσεις του κλάσματος εξώθησης της αριστερής κοιλίας πρέπει επίσης να λαμβάνονται υπόψη όταν ο ασθενής λαμβάνει θεραπεία με sunitinib. Σε ασθενείς χωρίς καρδιακούς παράγοντες κινδύνου, θα πρέπει να συνεχιστεί η αξιολόγηση του κλάσματος της κοιλιακής εξώθησης κατά την έναρξη.
Παρουσία κλινικών εκδηλώσεων CHF, συνιστάται η διακοπή της θεραπείας με sunitinib. Η χορήγηση Sunitinib θα πρέπει να διακοπεί ή / και να μειωθεί η δόση σε ασθενείς χωρίς κλινικά στοιχεία συμφορητικής καρδιακής ανεπάρκειας αλλά με μείωση του κλάσματος εξώθησης μεταξύ 20% και 50% από την αρχική γραμμή.
Επιμήκυνση του διαστήματος QT
Δεδομένα από προκλινικές μελέτες (in vitro Και in vivo), που διεξήχθη με δόσεις υψηλότερες από αυτές που συνιστώνται στους ανθρώπους, υποδεικνύουν ότι το sunitinib μπορεί να αναστείλει τις διαδικασίες καρδιακής επαναπόλωσης (π.χ. παράταση του διαστήματος QT).
Αυξήσεις στο διάστημα QTc σε περισσότερα από 500 msec σημειώθηκαν με ρυθμό 0,5% και αλλαγές από την αρχική τιμή άνω των 60 msec σημειώθηκαν στο 1,1% των 450 ασθενών με συμπαγείς όγκους. Και οι δύο αυτές παράμετροι αναγνωρίζονται ως δυνητικά σημαντικές παραλλαγές. Σε συγκεντρώσεις που αντιστοιχούν σε περίπου διπλάσιες θεραπευτικές συγκεντρώσεις, το sunitinib βρέθηκε ότι παρατείνει το διάστημα QTcF (διορθώθηκε σύμφωνα με τον τύπο της Frederica).
Η παράταση του διαστήματος QT μελετήθηκε σε μια μελέτη που περιελάμβανε 24 ασθενείς, ηλικίας 20-87 ετών, με προχωρημένες κακοήθειες. Τα αποτελέσματα αυτής της μελέτης έδειξαν ότι η sunitinib είχε επίδραση στο διάστημα QTc (ορίζεται ως προσαρμοσμένη στο εικονικό φάρμακο μέση αλλαγή> 10 msec, με ένα ανώτατο όριο 90% CI> 15 msec) σε θεραπευτική συγκέντρωση (ημέρα 3) χρησιμοποιώντας τη μέθοδο διόρθωσης βάσης 24 ωρών και στις συγκεντρώσεις παραπάνω σε θεραπευτικές (ημέρα 9) χρησιμοποιώντας και τις δύο μεθόδους διόρθωσης στην αρχή. Κανένας ασθενής δεν ανέφερε τιμή QTc> 500 msec.Παρόλο που μια επίδραση στο διάστημα QTcF παρατηρήθηκε την ημέρα 3 24 ώρες μετά τη χορήγηση (δηλαδή με την αναμενόμενη θεραπευτική συγκέντρωση στο πλάσμα μετά τη συνιστώμενη αρχική δόση των 50 mg) με τη βασική μέθοδο διόρθωσης 24 ωρών, η κλινική σημασία αυτού του ευρήματος είναι ασαφής Το
Χρησιμοποιώντας ολοκληρωμένες σειριακές αξιολογήσεις ΗΚΓ που αντιστοιχούν σε θεραπευτικές εκθέσεις ή εκθέσεις πάνω από θεραπευτικές, κανένας από τους ασθενείς στους αξιολογήσιμους πληθυσμούς ή τους πληθυσμούς ITT δεν παρατηρήθηκε παράταση του "σοβαρού" διαστήματος QTc (επομένως ίσο ή μεγαλύτερο από
Βαθμός 3 της έκδοσης CTCAE 3.0).
Σε θεραπευτικές συγκεντρώσεις πλάσματος, η μέση μέγιστη μεταβολή στο διάστημα QTcF (διορθώθηκε με τον τύπο της Frederica) από την αρχική τιμή ήταν 9,6 msec (90% CI 15,1 msec). Σε θεραπευτικές συγκεντρώσεις που αντιστοιχούν περίπου στις διπλάσιες των θεραπευτικών συγκεντρώσεων, η μέγιστη αλλαγή στο διάστημα QTcF από την αρχική τιμή ήταν 15,4 msec (90% CI 22,4 msec).
Η μοξιφλοξασίνη (400 mg) που χρησιμοποιήθηκε ως θετικός μάρτυρας παρουσίασε μέση μέγιστη μεταβολή στο διάστημα QTcF από την αρχική τιμή των 5,6 msec. Κανένα άτομο δεν ανέφερε επίδραση στο διάστημα QTc μεγαλύτερο από το βαθμό 2 (CTCAE έκδοση 3.0).
Η παράταση του διαστήματος QT μπορεί να προκαλέσει αυξημένο κίνδυνο κοιλιακών αρρυθμιών, συμπεριλαμβανομένου του Torsade de Pointes. Το Torsade de Pointes έχει παρατηρηθεί σε
Το Sunitinib θα πρέπει να χρησιμοποιείται με προσοχή σε ασθενείς με ιστορικό παράτασης του διαστήματος QT, σε ασθενείς που λαμβάνουν αντιαρρυθμικά ή με φαρμακευτικά προϊόντα που μπορούν να παρατείνουν το διάστημα QT ή σε ασθενείς με προϋπάρχουσες σχετικές καρδιακές παθήσεις, βραδυκαρδία ή ανωμαλίες. Η συγχορήγηση σουνιτινίμπης με ισχυρούς αναστολείς του CYP3A4 θα πρέπει να είναι περιορισμένη λόγω της πιθανής αύξησης των συγκεντρώσεων της σουνιτινίμπης στο πλάσμα (βλέπε παραγράφους 4.2 και 4.5).
Φλεβικά θρομβοεμβολικά επεισόδια
Φλεβικά θρομβοεμβολικά επεισόδια που σχετίζονται με τη θεραπεία παρατηρήθηκαν σε περίπου 1,0% των ασθενών με στερεούς όγκους που έλαβαν θεραπεία με sunitinib σε κλινικές μελέτες, συμπεριλαμβανομένων των μελετών GIST και MRCC.
Σε μια φάση 3 της μελέτης GIST, επτά ασθενείς (3%) που έλαβαν sunitinib και κανένας ασθενής στην ομάδα του εικονικού φαρμάκου δεν παρουσίασε φλεβικά θρομβοεμβολικά επεισόδια. πέντε από τους επτά ασθενείς είχαν βαθιά φλεβική θρόμβωση βαθμού 3 (DVT) και δύο είχαν βαθιά φλεβική θρόμβωση βαθμού 1 ή 2. Τέσσερις από αυτούς τους επτά ασθενείς που έλαβαν θεραπεία για GIST διέκοψαν μετά από παρατήρηση DVT.
Δεκατρείς ασθενείς (3%) έλαβαν σουνιτινίμπη στη μελέτη φάσης 3 του MRCC και δεν είχαν λάβει προηγούμενη θεραπεία και τέσσερις ασθενείς (2%) από τις δύο ανθεκτικές σε κυτταροκίνες μελέτες MRCC ανέφεραν φλεβικά θρομβοεμβολικά επεισόδια. Εννέα από αυτούς τους ασθενείς είχαν φλεβικά θρομβοεμβολικά επεισόδια. πνευμονική εμβολή, ένας με βαθμό 2 και οκτώ με βαθμό 4. Οκτώ από αυτούς τους ασθενείς είχαν DVT, έναν με βαθμό 1, δύο με βαθμό 2, τέσσερις με βαθμό 3 και έναν με βαθμό 4. Σε ασθενή με πνευμονική εμβολή στη μελέτη MRCC , ανθεκτική στις κυτοκίνες, η δόση διακόπηκε.
Από τους προηγουμένως μη θεραπευμένους ασθενείς με MRCC σε IFN-α, έξι (2%) ανέφεραν φλεβικά θρομβοεμβολικά επεισόδια, ένας ασθενής (πνευμονική εμβολή, όλα βαθμού 4).
Φλεβικά θρομβοεμβολικά επεισόδια αναφέρθηκαν για 1 (1,2%) ασθενή στο σκέλος sunitinib και 5 (6,1%) ασθενείς στο σκέλος του εικονικού φαρμάκου στη μελέτη pNET φάσης 3. Δύο από αυτά τα άτομα που έλαβαν εικονικό φάρμακο ανέφεραν DVT, ένα βαθμό 2 και ένα βαθμό 3.
Δεν παρατηρήθηκαν περιπτώσεις με θανατηφόρο αποτέλεσμα στις βασικές μελέτες των GIST, MRCC και pNET. Έχουν παρατηρηθεί περιπτώσεις με θανατηφόρα αποτελέσματα στο περιβάλλον μετά την κυκλοφορία του προϊόντος (βλέπε αναπνευστικά επεισόδια και παράγραφο 4.8).
Αρτηριακά θρομβοεμβολικά συμβάντα
Περιπτώσεις αρτηριακών θρομβοεμβολικών επεισοδίων (ΑΤΕ), μερικές φορές θανατηφόρες, έχουν αναφερθεί σε ασθενείς που έλαβαν θεραπεία με σουνιτινίμπη. Τα πιο συχνά περιστατικά περιλάμβαναν εγκεφαλοαγγειακό ατύχημα, παροδικό ισχαιμικό επεισόδιο και εγκεφαλική ισχαιμία. Παράγοντες κινδύνου που σχετίζονται με αρτηριακά θρομβοεμβολικά επεισόδια, εκτός από την προϋπάρχουσα κακοήθεια και την ηλικία 65 ετών και άνω, περιλάμβαναν υπέρταση, σακχαρώδη διαβήτη και προηγούμενο θρομβοεμβολικό συμβάν.
Αναπνευστικά γεγονότα
Ασθενείς που είχαν «πνευμονική εμβολή εντός των προηγούμενων 12 μηνών αποκλείστηκαν από κλινικές δοκιμές με sunitinib.
Σε ασθενείς που έλαβαν sunitinib στη βασική μελέτη φάσης 3, πνευμονικά συμβάντα (δύσπνοια, υπεζωκοτική συλλογή, πνευμονική εμβολή ή πνευμονικό οίδημα) παρατηρήθηκαν σε περίπου 17,8% των ασθενών με GIST, σε περίπου 26,7% από αυτούς με MRCC και σε 12% ασθενείς με pNET.
Περίπου το 22,2% των ασθενών με συμπαγείς όγκους, συμπεριλαμβανομένου του GIST και του MRCC, που έλαβαν θεραπεία με sunitinib σε κλινικές μελέτες ανέφεραν πνευμονικά επεισόδια.
Περιπτώσεις πνευμονικής εμβολής παρατηρήθηκαν σε περίπου 3,1% των ασθενών με GIST και περίπου 1,2% των ασθενών με MRCC που έλαβαν θεραπεία με sunitinib σε μελέτες φάσης 3 (βλ. Παράγραφο 4.4. - Φλεβικά θρομβοεμβολικά επεισόδια). Δεν παρατηρήθηκαν περιπτώσεις πνευμονικής εμβολής σε ασθενείς με pNET υποβλήθηκαν σε θεραπεία με sunitinib στη μελέτη φάσης 3. Σπάνιες περιπτώσεις με θανατηφόρο αποτέλεσμα έχουν παρατηρηθεί στο περιβάλλον μετά την κυκλοφορία (βλ. παράγραφο 4.8).
Δυσλειτουργία του θυρεοειδούς
Συνιστάται η αξιολόγηση της λειτουργίας του θυρεοειδούς μετρώντας τις βασικές εργαστηριακές τιμές σε όλους τους ασθενείς. Ασθενείς με προϋπάρχον υποθυρεοειδισμό ή υπερθυρεοειδισμό θα πρέπει να αντιμετωπίζονται σύμφωνα με την τυπική κλινική πρακτική πριν από την έναρξη της θεραπείας με sunitinib. Κατά τη διάρκεια της θεραπείας με sunitinib, πρέπει να γίνεται τακτικός έλεγχος της λειτουργίας του θυρεοειδούς κάθε 3 μήνες. Επιπλέον, όλοι οι ασθενείς θα πρέπει να παρακολουθούνται στενά κατά τη διάρκεια της θεραπείας για πιθανά σημεία και συμπτώματα δυσλειτουργίας του θυρεοειδούς και οι ασθενείς που εμφανίζουν οποιεσδήποτε ενδείξεις ή / και συμπτώματα ενδεικτικά δυσλειτουργίας του θυρεοειδούς θα πρέπει να υποβάλλονται σε εργαστηριακό έλεγχο της λειτουργίας του θυρεοειδούς όπως αναμενόταν κλινικά. Οι ασθενείς που αναπτύσσουν δυσλειτουργία του θυρεοειδούς πρέπει να αντιμετωπίζονται σύμφωνα με την τυπική κλινική πρακτική.
Έχει παρατηρηθεί ότι υποθυρεοειδισμός εμφανίζεται στην αρχή ή στο τέλος της θεραπείας με sunitinib.
Ο υποθυρεοειδισμός αναφέρθηκε ως ανεπιθύμητη ενέργεια σε 7 ασθενείς (4%) που έλαβαν σουνιτινίμπη στις δύο μελέτες MRCC που διεξήχθησαν σε ανθεκτικούς ασθενείς σε κυτοκίνες. Σε 61 ασθενείς (16%) που έλαβαν σουνιτινίμπη και σε τρεις ασθενείς (
Επιπλέον, αναφέρθηκαν αυξήσεις της TSH σε 4 ασθενείς (2%) που έλαβαν θεραπεία για ανθεκτικό στην κυτοκίνη MRCC. Συνολικά, το 7% του πληθυσμού του MRCC ανέφερε κλινικά ή εργαστηριακά στοιχεία υποθυρεοειδισμού που σχετίζεται με τη θεραπεία. Ο επίκτητος υποθυρεοειδισμός παρατηρήθηκε στο 6,2% των ασθενών στη μελέτη GIST που έλαβαν sunitinib σε σύγκριση με το 1% στην ομάδα του εικονικού φαρμάκου. Στη μελέτη Φάσης 3 pNET, υποθυρεοειδισμός αναφέρθηκε σε 6 ασθενείς (7,2%) που έλαβαν σουνιτινίμπη και σε έναν ασθενή (1,2%) που έλαβε εικονικό φάρμακο.
Η λειτουργία του θυρεοειδούς παρακολουθήθηκε προοπτικά σε δύο μελέτες σε ασθενείς με καρκίνο του μαστού. Το SUTENT δεν έχει εγκριθεί για τη θεραπεία του καρκίνου του μαστού. Σε μία μελέτη, υποθυρεοειδισμός αναφέρθηκε σε 15 άτομα (13,6%) που έλαβαν sunitinib και σε 3 άτομα (2,9%) που έλαβαν τυπική θεραπεία. Αυξημένη TSH αίματος αναφέρθηκε σε 1 άτομο. (0,9%) που έλαβαν sunitinib και σε κανένα άτομο αντιμετωπίζονται με τυπική θεραπεία. Ο υπερθυρεοειδισμός δεν αναφέρθηκε σε κανένα από τα άτομα που έλαβαν sunitinib και αναφέρθηκε σε 1 άτομο (1,0%) που έλαβε τυπική θεραπεία. Στην άλλη μελέτη, υποθυρεοειδισμός αναφέρθηκε σε συνολικά 31 άτομα (13%) που έλαβαν sunitinib και 2 άτομα (0,8%) έλαβαν καπεσιταβίνη.Αυξημένη TSH αίματος αναφέρθηκε σε 12 άτομα (5,0%) που έλαβαν σουνιτινίμπη και σε κανένα άτομο που έλαβε καπεσιταβίνη. Αναφέρθηκε υπερθυρεοειδισμός σε 4 άτομα (1,7%) που έλαβαν sunitinib και σε κανένα άτομο που έλαβε καπεσιταβίνη. Μειωμένη TSH αίματος αναφέρθηκε σε 3 άτομα (1,3%) που έλαβαν sunitinib και σε κανένα άτομο. Έλαβαν θεραπεία με capecitabine. Αναφέρθηκε αύξηση T4 σε 2 άτομα (0,8%) έλαβαν σουνιτινίμπη και σε 1 άτομο (0,4%) έλαβαν καπεσιταβίνη. Η αύξηση της Τ3 αναφέρθηκε σε 1 άτομο (0,8%) που έλαβε σουνιτινίμπη και σε κανένα άτομο που δεν έλαβε καπεσιταβίνη. Όλα τα σχετιζόμενα με το θυρεοειδή συμβάντα που αναφέρθηκαν ήταν βαθμού 1-2.
Περιπτώσεις υπερθυρεοειδισμού, μερικές ακολουθούμενες από υποθυρεοειδισμό και περιπτώσεις θυρεοειδίτιδας έχουν αναφερθεί σπάνια σε κλινικές δοκιμές και στη φάση εμπορίας του προϊόντος.
Παγκρεατίτιδα
Αυξήσεις στη δραστηριότητα της λιπάσης του ορού και της αμυλάσης έχουν παρατηρηθεί σε ασθενείς με αρκετούς στερεούς όγκους που λαμβάνουν sunitinib. Οι αυξήσεις της δραστηριότητας της λιπάσης στον ορό ήταν παροδικές και γενικά δεν σχετίζονται με σημεία και συμπτώματα παγκρεατίτιδας σε άτομα με συμπαγείς όγκους διαφόρων τύπων.
Η παγκρεατίτιδα παρατηρήθηκε ασυνήθιστα (
Έχουν αναφερθεί περιπτώσεις σοβαρών παγκρεατικών συμβάντων, μερικές με θανατηφόρο έκβαση.
Εάν εμφανιστούν συμπτώματα παγκρεατίτιδας, η θεραπεία με σουνιτινίμπη θα πρέπει να διακοπεί και να παρέχεται στους ασθενείς επαρκής υποστηρικτική φροντίδα. Δεν αναφέρθηκαν συμβάντα παγκρεατίτιδας που σχετίζονται με τη θεραπεία στη μελέτη Φάσης 3 pNET.
Ηπατοτοξικότητα
Παρατηρήθηκε ηπατοτοξικότητα σε ασθενείς που έλαβαν sunitinib. Περιπτώσεις ηπατικής ανεπάρκειας, μερικές φορές με θανατηφόρο αποτέλεσμα, έχουν παρατηρηθεί στη λειτουργία του ήπατος (τρανσαμινάση αλανίνης [ALT], ασπαρτική τρανσαμινάση [AST], επίπεδα χολερυθρίνης). Σημεία ή συμπτώματα ηπατικής ανεπάρκειας, Η θεραπεία με sunitinib πρέπει να διακοπεί και να παρέχεται στους ασθενείς η κατάλληλη υποστηρικτική ιατρική φροντίδα.
Ηπατοχολικές διαταραχές
Η θεραπεία με σουνιτινίμπη μπορεί να σχετίζεται με χολοκυστίτιδα, συμπεριλαμβανομένης της αλιθιακής χολοκυστίτιδας και της ενφθεματικής χολοκυστίτιδας. Σε βασικές κλινικές μελέτες, η συχνότητα χολοκυστίτιδας ήταν 0,5%.
Έχουν αναφερθεί περιπτώσεις χολοκυστίτιδας στο περιβάλλον μετά την κυκλοφορία.
Νεφρική λειτουργία
Έχουν αναφερθεί περιπτώσεις νεφρικής δυσλειτουργίας, νεφρικής ανεπάρκειας ή / και οξείας νεφρικής ανεπάρκειας, σε ορισμένες περιπτώσεις με θανατηφόρο έκβαση.
Παράγοντες κινδύνου που σχετίζονται με νεφρική δυσλειτουργία σε ασθενείς που λαμβάνουν σουνιτινίμπη περιλάμβαναν, εκτός από το προϋπάρχον καρκίνωμα των νεφρικών κυττάρων: προχωρημένη ηλικία, σακχαρώδης διαβήτης, προϋπάρχουσα νεφρική δυσλειτουργία, καρδιακή ανεπάρκεια, υπέρταση, σήψη, αφυδάτωση / υποογκαιμία και ραβδομυόλυση.
Η ασφάλεια της συνέχισης της θεραπείας με sunitinib σε ασθενείς με μέτρια έως σοβαρή πρωτεϊνουρία δεν έχει αξιολογηθεί συστηματικά.
Έχουν αναφερθεί περιπτώσεις πρωτεϊνουρίας και σπάνιες περιπτώσεις νεφρωσικού συνδρόμου. Η βασική ανάλυση ούρων συνιστάται και οι ασθενείς πρέπει να παρακολουθούνται για πιθανή ανάπτυξη ή επιδείνωση της πρωτεϊνουρίας.
Η θεραπεία με Sunitinib θα πρέπει να διακοπεί σε ασθενείς με νεφρωσικό σύνδρομο.
Συρίγγια
Εάν εμφανιστεί σχηματισμός συριγγίου, η θεραπεία με sunitinib θα πρέπει να διακοπεί. Υπάρχουν περιορισμένες διαθέσιμες πληροφορίες για παρατεταμένη θεραπεία με sunitinib σε ασθενείς που παρουσιάζουν συρίγγια.
Διαταραχή της διαδικασίας επούλωσης πληγών
Έχουν αναφερθεί περιπτώσεις μειωμένης επούλωσης πληγών κατά τη διάρκεια της θεραπείας με sunitinib. Δεν έχουν διεξαχθεί επίσημες κλινικές μελέτες σχετικά με την επίδραση του sunitinib στην επούλωση τραυμάτων. Για προληπτικούς λόγους συνιστάται η προσωρινή διακοπή της θεραπείας με sunitinib σε ασθενείς που υποβάλλονται σε σημαντική χειρουργική επέμβαση. Κλινική εμπειρία σχετικά με το χρόνο που απαιτείται για την επανεκκίνηση. Επομένως, η απόφαση για επανέναρξη της θεραπείας με sunitinib μετά από σημαντική χειρουργική επέμβαση πρέπει να βασίζεται στην κλινική κρίση της ανάρρωσης από τη χειρουργική επέμβαση.
Οστεονέκρωση της κάτω γνάθου / άνω γνάθου
Έχουν αναφερθεί περιπτώσεις οστεονέκρωσης της γνάθου σε ασθενείς που έλαβαν SUTENT. Στην πλειονότητα των αναφερόμενων περιπτώσεων, οι ασθενείς είχαν λάβει προηγούμενη ή ταυτόχρονη θεραπεία με ενδοφλέβια διφωσφονικά, με τα οποία η οστεονέκρωση της γνάθου είναι αναγνωρισμένος κίνδυνος. Επομένως, πρέπει να δίνεται προσοχή όταν χορηγούνται ταυτόχρονα ή συνδυαστικά διφωσφονικά SUTENT ή συνδυαστικά.
Οι επεμβατικές οδοντιατρικές παρεμβάσεις έχουν επίσης προσδιοριστεί ως παράγοντας κινδύνου. Πριν από τη θεραπεία με SUTENT πρέπει να εξεταστεί η οδοντιατρική εξέταση και η κατάλληλη προληπτική οδοντιατρική φροντίδα. Εάν είναι δυνατόν, οι επεμβατικές οδοντιατρικές παρεμβάσεις θα πρέπει να αποφεύγονται σε ασθενείς που έχουν λάβει προηγουμένως ή λαμβάνουν διφωσφονικά ενδοφλέβια (βλ. Παράγραφο 4.8).
Υπερευαισθησία / αγγειοοίδημα
Εάν εμφανιστεί οίδημα λόγω αντίδρασης υπερευαισθησίας, η θεραπεία με sunitinib πρέπει να διακοπεί και να χορηγηθεί τυπική ιατρική θεραπεία.
Διαταραχές του νευρικού συστήματος
Διαταραχές γεύσης
Δυσγευσία αναφέρθηκε σε περίπου 28% των ασθενών που έλαβαν sunitinib κατά τη διάρκεια κλινικών δοκιμών.
Σπασμοί
Σε κλινικές δοκιμές με sunitinib και μετά την κυκλοφορία, έχουν παρατηρηθεί περιπτώσεις κρίσεων σε άτομα με ή χωρίς ακτινολογικές ενδείξεις εγκεφαλικών μεταστάσεων. Επιπλέον, υπήρξε περιορισμένος αριθμός αναφορών (πονοκέφαλος, μειωμένη εγρήγορση, διαταραχή της ψυχικής λειτουργίας και απώλεια της όρασης, συμπεριλαμβανομένης της τύφλωσης του φλοιού, θα πρέπει να ελέγχονται με ιατρική θεραπεία, συμπεριλαμβανομένου του ελέγχου της υπέρτασης. Συνιστάται η προσωρινή διακοπή του sunitinib. εάν συμβεί, η θεραπεία μπορεί να επαναληφθεί κατά την κρίση του θεράποντος ιατρού.
Σύνδρομο λύσης όγκου (TLS)
Περιπτώσεις συνδρόμου λύσης όγκου (TLS), μερικές με θανατηφόρο αποτέλεσμα, έχουν παρατηρηθεί σπάνια σε κλινικές μελέτες και έχουν αναφερθεί μετά την κυκλοφορία σε ασθενείς που έλαβαν sunitinib. Οι παράγοντες κινδύνου για TLS περιλαμβάνουν υψηλό φορτίο όγκου, προϋπάρχουσα χρόνια νεφρική ανεπάρκεια, ολιγουρία, αφυδάτωση, υπόταση και όξινα ούρα. Αυτοί οι ασθενείς θα πρέπει να παρακολουθούνται προσεκτικά και να αντιμετωπίζονται όπως υποδεικνύεται κλινικά · για αυτούς τους ασθενείς θα πρέπει να λαμβάνεται υπόψη η προφυλακτική ενυδάτωση.
Λοιμώξεις
Έχουν αναφερθεί περιπτώσεις σοβαρών λοιμώξεων, με ή χωρίς ουδετεροπενία, συμπεριλαμβανομένων ορισμένων περιπτώσεων με θανατηφόρο έκβαση.
Οι λοιμώξεις που παρατηρούνται συχνότερα με τη θεραπεία με sunitinib είναι λοιμώξεις τυπικές για τον καρκινοπαθή, όπως αναπνευστική, ουροφόρος οδός, δέρμα και σηψαιμία.
Έχουν αναφερθεί σπάνιες, μερικές φορές θανατηφόρες, περιπτώσεις νεκρωτικής απονευρωσίτιδας, συμπεριλαμβανομένης αυτής του περινέου. Η θεραπεία με Sunitinib θα πρέπει να διακοπεί σε ασθενείς που αναπτύσσουν νεκρωτική απονευρωσίτιδα και η κατάλληλη θεραπεία να ξεκινήσει αμέσως.
Υπογλυκαιμία
Έχουν αναφερθεί μειωμένα επίπεδα γλυκόζης στο αίμα κατά τη διάρκεια της θεραπείας με sunitinib, μερικά από αυτά είναι κλινικά συμπτωματικά και απαιτούν νοσηλεία λόγω απώλειας συνείδησης. Σε περίπτωση συμπτωματικής υπογλυκαιμίας, η θεραπεία με sunitinib θα πρέπει να διακοπεί προσωρινά. Τα επίπεδα γλυκόζης αίματος πρέπει να ελέγχονται τακτικά σε διαβητικούς ασθενείς για να εκτιμηθεί εάν η δοσολογία των φαρμάκων για τον διαβήτη πρέπει να προσαρμοστεί ώστε να ελαχιστοποιηθεί ο κίνδυνος υπογλυκαιμίας.
04.5 Αλληλεπιδράσεις με άλλα φαρμακευτικά προϊόντα και άλλες μορφές αλληλεπίδρασης
Μελέτες αλληλεπίδρασης έχουν πραγματοποιηθεί μόνο σε ενήλικες.
Φάρμακα που μπορούν να αυξηθεί συγκεντρώσεις του sunitinib στο πλάσμα
Σε υγιείς εθελοντές, η συγχορήγηση μίας δόσης sunitinib με κετοκοναζόλη, έναν ισχυρό αναστολέα του CYP3A4, είχε ως αποτέλεσμα την αύξηση του συνδυασμένου [sunitinib + πρωτοπαθούς μεταβολίτη] Cmax και AUC0-∞ κατά 49% και 51%, αντίστοιχα.
Χορήγηση σουνιτινίμπης με ισχυρούς αναστολείς του CYP3A4 (π.χ. ριτοναβίρη , ιτρακοναζόλη, ερυθρομυκίνη, κλαριθρομυκίνη, χυμός γκρέιπφρουτ) μπορεί να αυξήσουν τις συγκεντρώσεις sunitinib.
Συνεπώς, θα πρέπει να αποφεύγεται ο συνδυασμός με αναστολείς του CYP3A4 ή θα πρέπει να εξεταστεί ένα εναλλακτικό φαρμακευτικό προϊόν χωρίς ή ελάχιστη δυνατότητα αναστολής του CYP3A4.
Εάν αυτό δεν είναι δυνατό, η δόση του SUTENT μπορεί να χρειαστεί να μειωθεί σε τουλάχιστον 37,5 mg / ημέρα για GIST και MRCC ή 25 mg / ημέρα για pNET, βάσει προσεκτικής παρακολούθησης της ανεκτικότητας (βλ. Παράγραφο 4.2).
Φάρμακα που μπορούν περιορίζω συγκεντρώσεις του sunitinib στο πλάσμα
Σε υγιείς εθελοντές, η συγχορήγηση μίας δόσης σουνιτινίμπης και ριφαμπικίνης επαγωγέα CYP3A4 είχε ως αποτέλεσμα τη μείωση της συνδυασμένης [sunitinib + πρωτοπαθούς μεταβολίτης] Cmax και AUC0-∞ κατά 23% και 46%, αντίστοιχα.
Χορήγηση σουνιτινίμπης με ισχυρούς επαγωγείς του CYP3A4 (π.χ. δεξαμεθαζόνη, φαινυτοΐνη, καρβαμαζεπίνη, ριφαμπικίνη, φαινοβαρβιτάλη ή φυτικά παρασκευάσματα που περιέχουν St John's wort /Hypericum perforatum) μπορεί να μειώσει τις συγκεντρώσεις sunitinib. Συνεπώς, η συσχέτιση με επαγωγείς του CYP3A4 θα πρέπει να αποφεύγεται ή θα πρέπει να εξεταστεί ένα εναλλακτικό φαρμακευτικό προϊόν χωρίς ή ελάχιστη δυνατότητα να προκαλέσει το CYP3A4. έως 87,5 mg / ημέρα για GIST και MRCC ή 62,5 mg / ημέρα για pNET) με βάση την προσεκτική παρακολούθηση της ανεκτικότητας (βλ. παράγραφο 4.2).
04.6 Κύηση και γαλουχία
Εγκυμοσύνη
Δεν έχουν διεξαχθεί μελέτες σε έγκυες γυναίκες που λαμβάνουν sunitinib. Μελέτες σε ζώα έχουν δείξει τοξικότητα στην αναπαραγωγή, συμπεριλαμβανομένων των εμβρυϊκών δυσπλασιών (βλ. Παράγραφο 5.3).
Το SUTENT δεν πρέπει να χρησιμοποιείται κατά τη διάρκεια της εγκυμοσύνης ή σε γυναίκες που δεν χρησιμοποιούν αποτελεσματικά αντισυλληπτικά μέτρα, εκτός εάν τα πιθανά οφέλη δικαιολογούν τον πιθανό κίνδυνο για το έμβρυο. Εάν το SUTENT χρησιμοποιείται κατά τη διάρκεια της εγκυμοσύνης ή εάν η ασθενής μείνει έγκυος κατά τη διάρκεια της θεραπείας με SUTENT, ο ασθενής θα πρέπει να ενημερώνεται για τους πιθανούς κινδύνους για το έμβρυο.
Οι γυναίκες σε αναπαραγωγική ηλικία πρέπει να συμβουλεύονται να χρησιμοποιούν αποτελεσματική αντισύλληψη και να αποφεύγουν να μείνουν έγκυες όταν λαμβάνουν θεραπεία με SUTENT.
Ωρα ταίσματος
Το sunitinib και / ή οι μεταβολίτες του απεκκρίνονται στο γάλα αρουραίων. Είναι άγνωστο εάν το sunitinib ή ο κύριος ενεργός μεταβολίτης του απεκκρίνονται στο ανθρώπινο γάλα. Δεδομένου ότι οι δραστικές ουσίες απεκκρίνονται γενικά στο μητρικό γάλα και λαμβάνοντας υπόψη τις πιθανές σοβαρές ανεπιθύμητες ενέργειες σε θηλάζοντα βρέφη, οι γυναίκες δεν πρέπει να θηλάζουν κατά τη διάρκεια της θεραπείας με SUTENT.
Γονιμότητα
Προκλινικά δεδομένα υποδηλώνουν ότι η γονιμότητα ανδρών και γυναικών μπορεί να επηρεαστεί από τη θεραπεία με sunitinib (βλ. Παράγραφο 5.3).
04.7 Επιδράσεις στην ικανότητα οδήγησης και χειρισμού μηχανών
Δεν έχουν διεξαχθεί μελέτες σχετικά με τις επιδράσεις στην ικανότητα οδήγησης και χειρισμού μηχανών. Οι ασθενείς θα πρέπει να ενημερώνονται για την πιθανή εμφάνιση ζάλης κατά τη διάρκεια της θεραπείας με sunitinib.
04.8 Ανεπιθύμητες ενέργειες
Περίληψη του προφίλ ασφαλείας
Οι πιο σοβαρές ανεπιθύμητες ενέργειες που σχετίζονται με τη θεραπεία με sunitinib, μερικές θανατηφόρες, είναι η νεφρική ανεπάρκεια, η καρδιακή ανεπάρκεια, η πνευμονική εμβολή, η διάτρηση του γαστρεντερικού και οι αιμορραγίες (π.χ. αιμορραγίες του αναπνευστικού, του γαστρεντερικού, του όγκου, των ούρων και του εγκεφάλου).
Οι πιο συχνές ανεπιθύμητες ενέργειες οποιουδήποτε βαθμού (αναφέρθηκαν από ασθενείς σε κεντρικές κλινικές δοκιμές για RCC, GIST και pNET) περιελάμβαναν μειωμένη όρεξη, διαταραχές γεύσης, υπέρταση, κόπωση, γαστρεντερικές διαταραχές (π.χ. διάρροια, ναυτία, στοματίτιδα, δυσπεψία και έμετος), αποχρωματισμό του συνδρόμου δέρματος και παλάμης-πελματιαίας ερυθροδυσαισθησίας. Αυτά τα συμπτώματα μπορεί να μειωθούν με τη συνέχιση της θεραπείας. Ο υποθυρεοειδισμός μπορεί να προκύψει κατά τη διάρκεια της θεραπείας. Αιματολογικές διαταραχές (π.χ. ουδετεροπενία, θρομβοπενία και αναιμία) ήταν από τις πιο συχνές ανεπιθύμητες ενέργειες φαρμάκων.
Θανατηφόρες ανεπιθύμητες ενέργειες άλλες από αυτές που αναφέρονται στην ενότητα 4.4. ή στην ενότητα 4.8 και θεωρείται πιθανόν ότι σχετίζεται με το sunitinib περιλαμβάνουν ανεπάρκεια πολλαπλών οργάνων, διάχυτη ενδαγγειακή πήξη, περιτοναϊκή αιμορραγία, επινεφριδιακή ανεπάρκεια, πνευμοθώρακα, σοκ και αιφνίδιο θάνατο.
Πίνακας ανεπιθύμητων ενεργειών
Οι ανεπιθύμητες ενέργειες που αναφέρθηκαν από ασθενείς με GIST, MRCC και pNET σε ένα σύνολο δεδομένων 7115 ασθενών παρατίθενται παρακάτω και κατηγοριοποιούνται ανά κατηγορία οργάνου συστήματος, συχνότητα και σοβαρότητα (NCI-CTCAE). Αναφέρονται επίσης ανεπιθύμητες ενέργειες μετά την κυκλοφορία που εντοπίστηκαν σε κλινικές μελέτες. Σε κάθε κατηγορία συχνοτήτων, αναφέρονται ανεπιθύμητες ενέργειες με σειρά φθίνουσας σοβαρότητας.
Οι συχνότητες ορίζονται ως εξής: πολύ συχνές (≥1 / 10), κοινές (≥1 / 100a
Πίνακας 1 - Ανεπιθύμητες ενέργειες που αναφέρθηκαν σε κλινικές μελέτες
Οι παρακάτω όροι έχουν ομαδοποιηθεί:
ρινοφαρυγγίτιδα και έρπης του στόματος
β Βρογχίτιδα, λοίμωξη του κατώτερου αναπνευστικού συστήματος, πνευμονία και λοίμωξη του αναπνευστικού συστήματος
γ Απόστημα, απόστημα άκρων, απόστημα πρωκτού, απόστημα ούλων, απόστημα ήπατος, απόστημα παγκρέατος, περινεϊκό απόστημα, περιμετρικό απόστημα, απόστημα ορθού, υποδόριο απόστημα και οδοντικό απόστημα
d Οισοφαγική καντιντίαση και στοματική καντιντίαση
και κυτταρίτιδα και λοίμωξη του δέρματος
στ Σήψη και σηπτικό σοκ
g Κοιλιακό απόστημα, κοιλιακή σήψη, εκκολπωματίτιδα και οστεομυελίτιδα
h Μειωμένη όρεξη και ανορεξία
i Δυσγευσία, ageusia και αλλοίωση της γεύσης
j Οξύ στεφανιαίο σύνδρομο, στηθάγχη, ασταθής στηθάγχη, απόφραξη στεφανιαίας αρτηρίας, ισχαιμία του μυοκαρδίου
k Μείωση / ανωμαλία του κλάσματος εκτίναξης
l Οξύ έμφραγμα του μυοκαρδίου, έμφραγμα του μυοκαρδίου, σιωπηλό έμφραγμα του μυοκαρδίου
m Οροφαρυγγικός και φαρυγγολαρυγγικός πόνος
n Στοματίτιδα και αφθώδη στοματίτιδα
o Κοιλιακός πόνος, πόνος στην κάτω και άνω κοιλιακή χώρα
p Γαστρεντερική και εντερική διάτρηση
q Χολοκυστίτιδα και αλιθική χολοκυστίτιδα
r Κίτρινο δέρμα, δυσχρωμίες και δυσχρωμίες του δέρματος
s oriωριασική δερματίτιδα, απολεπιστικό εξάνθημα, εξάνθημα, ερυθηματώδες εξάνθημα, ωοθυλακικό εξάνθημα, γενικευμένο εξάνθημα, εξάνθημα της ωχράς κηλίδας, εξάνθημα της ωχράς κηλίδας, βλατίδιο εξάνθημα και κνησμώδες εξάνθημα
t Δερματική αντίδραση και παθολογία του δέρματος
u Παθολογία των νυχιών και αποχρωματισμός των νυχιών
v Κούραση και ασθένεια
w Οίδημα προσώπου, οίδημα και περιφερικό οίδημα
x Αμυλάση και αυξημένη αμυλάση
* Περιλαμβάνει μοιραία γεγονότα
Περιγραφή των ανεπιθύμητων ενεργειών που εντοπίστηκαν
Λοιμώξεις και προσβολές: Έχουν αναφερθεί περιπτώσεις σοβαρών λοιμώξεων (με ή χωρίς ουδετεροπενία), συμπεριλαμβανομένων περιπτώσεων με θανατηφόρο έκβαση. Έχουν αναφερθεί περιπτώσεις νεκρωτικής απονευρωσίτιδας, μερικές φορές θανατηφόρων, που θα μπορούσαν επίσης να επηρεάσουν την περιοχή του περινέου (βλ. Επίσης παράγραφο 4.4).
Διαταραχές του αίματος και του λεμφικού συστήματος: Έχουν αναφερθεί περιπτώσεις θρομβωτικής μικροαγγειοπάθειας. Σε αυτές τις περιπτώσεις, συνιστάται η προσωρινή αναστολή του SUTENT. μετά την επίλυση αυτών των συμβάντων, η θεραπεία μπορεί να ξεκινήσει εκ νέου κατά την κρίση του θεράποντος ιατρού.
Διαταραχές του ανοσοποιητικού συστήματος: Έχουν αναφερθεί αντιδράσεις υπερευαισθησίας, συμπεριλαμβανομένου του αγγειοοιδήματος.
Διαταραχές του νευρικού συστήματος: Λίγες περιπτώσεις, μερικές θανατηφόρες, των ατόμων που παρουσίασαν επιληπτικές κρίσεις και ακτινολογικά στοιχεία αναστρέψιμου συνδρόμου οπίσθιας λευκοεγκεφαλοπάθειας (RPLS) έχουν αναφερθεί (βλ. Επίσης παράγραφο 4.4).
Διαταραχές μεταβολισμού και διατροφής: Έχει αναφερθεί υψηλότερη συχνότητα υπογλυκαιμικών συμβάντων σε ασθενείς με pNET σε σύγκριση με ασθενείς με MRCC και GIST. Ωστόσο, πολλά από τα ανεπιθύμητα συμβάντα που παρατηρήθηκαν σε κλινικές δοκιμές δεν θεωρήθηκαν ότι σχετίζονται με τη θεραπεία της μελέτης.
Ηπατοχολικές διαταραχές: Έχει αναφερθεί ηπατική δυσλειτουργία και μπορεί να περιλαμβάνει ανωμαλίες δοκιμής ηπατικής λειτουργίας, ηπατίτιδα ή ηπατική ανεπάρκεια.
Διαταραχές του δέρματος και του υποδόριου ιστού: Έχουν αναφερθεί περιπτώσεις γάγγραινας πυοδερμίας, γενικά αναστρέψιμων μετά τη διακοπή της θεραπείας (βλ. Επίσης παράγραφο 4.4).
Διαταραχές του μυοσκελετικού και του συνδετικού ιστού: Έχουν αναφερθεί περιπτώσεις μυοπάθειας και / ή ραβδομυόλυσης, ορισμένες που σχετίζονται με οξεία νεφρική ανεπάρκεια. Οι ασθενείς που παρουσιάζουν σημεία ή συμπτώματα τοξικότητας των μυών πρέπει να αντιμετωπίζονται σύμφωνα με την τυπική ιατρική πρακτική.
Έχουν αναφερθεί περιπτώσεις σχηματισμού συριγγίου, που μερικές φορές σχετίζονται με νέκρωση και υποχώρηση όγκου, σε ορισμένες περιπτώσεις με θανατηφόρο έκβαση.
Έχουν αναφερθεί περιπτώσεις οστεονέκρωσης της γνάθου σε ασθενείς που έλαβαν SUTENT, πολλές από τις οποίες εμφανίστηκαν σε ασθενείς που είχαν αναγνωρίσει παράγοντες κινδύνου για οστεονέκρωση της γνάθου, ιδιαίτερα έκθεση σε ενδοφλέβια διφωσφονικά και / ή ιστορικό οδοντικής νόσου που απαιτούσε επεμβατικές οδοντιατρικές παρεμβάσεις (βλ. επίσης τμήμα 4.4).
Αναφορά ύποπτων ανεπιθύμητων ενεργειών
Η αναφορά ύποπτων ανεπιθύμητων ενεργειών που συνέβησαν μετά την έγκριση του φαρμακευτικού προϊόντος είναι σημαντική καθώς επιτρέπει τη συνεχή παρακολούθηση της ισορροπίας οφέλους / κινδύνου του φαρμακευτικού προϊόντος. Οι επαγγελματίες υγείας καλούνται να αναφέρουν τυχόν υποψίες ανεπιθύμητων ενεργειών μέσω του εθνικού συστήματος αναφοράς. Στο "Παράρτημα V Το
04,9 Υπερδοσολογία
Δεν υπάρχει ειδικό αντίδοτο στην υπερδοσολογία με sunitinib και η θεραπεία της υπερδοσολογίας πρέπει να περιλαμβάνει γενικά υποστηρικτικά μέτρα. Εάν ενδείκνυται, η αποβολή της μη απορροφημένης δραστικής ουσίας μπορεί να επιτευχθεί με έμετο ή πλύση στομάχου. Έχουν αναφερθεί. Περιπτώσεις υπερδοσολογίας. Σε ορισμένες σε αυτές τις περιπτώσεις, οι ανεπιθύμητες ενέργειες που προέκυψαν ήταν σύμφωνες με το γνωστό προφίλ ασφάλειας του sunitinib.
05.0 ΦΑΡΜΑΚΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ
05.1 Φαρμακοδυναμικές ιδιότητες
Φαρμακοθεραπευτική ομάδα: αντινεοπλασματικοί παράγοντες, αναστολείς πρωτεϊνικής κινάσης.
Κωδικός ATC: LO1XE04.
Μηχανισμός δράσης
Το Sunitinib αναστέλλει πολλαπλούς υποδοχείς τυροσίνης κινάσης (RTK) που εμπλέκονται στην ανάπτυξη του όγκου, στη νεοαγγειογένεση του όγκου και στη μεταστατική εξέλιξη του καρκίνου. Το Sunitinib έχει αναγνωριστεί ως αναστολέας των αιμοπεταλιακών παραγόντων αυξητικών παραγόντων (PDGFRα και PDGFRβ), των υποδοχέων αγγειακών ενδοθηλιακών αυξητικών παραγόντων (VEGFR1, VEGFR2 και VEGFR3), υποδοχέων παραγόντων βλαστικών κυττάρων (KIT), υποδοχέων κινάσης τυροσίνης FLT3 (Fms-like κινάση τυροσίνης 3), ο υποδοχέας CSF-1R (υποδοχέας διεγερτικού παράγοντα αποικίας (CSF-1R)) και του γλουιαίου προερχόμενου υποδοχέα ουδετερού παράγοντα (RET). Ο κύριος μεταβολίτης παρουσιάζει δραστικότητα συγκρίσιμη με εκείνη του sunitinib σε βιοχημικές και κυτταρικές δοκιμές.
Κλινική αποτελεσματικότητα και ασφάλεια
Η ασφάλεια και η κλινική αποτελεσματικότητα της σουνιτινίμπης μελετήθηκαν στη θεραπεία ασθενών με GIST ανθεκτικούς στην ιματινίμπη (δηλ. Εκείνους τους ασθενείς που είχαν προοδεύσει κατά τη διάρκεια ή μετά τη θεραπεία με ιματινίμπη) ή δυσανεξίας στην ιματινίμπη (δηλ. Εκείνους που είχαν σημαντική τοξικότητα κατά τη θεραπεία με ιματινίμπη) που απέτρεψε τη συνέχιση της θεραπείας), στη θεραπεία ασθενών με MRCC και στη θεραπεία ασθενών με μη λειτουργικό pNET.
Η αποτελεσματικότητα βασίζεται στο χρόνο έως την εξέλιξη του όγκου και την αύξηση της επιβίωσης σε ασθενείς με GIST, επιβίωση χωρίς εξέλιξη και ποσοστό αντικειμενικής ανταπόκρισης σε ασθενείς που δεν είχαν ήδη αντιμετωπιστεί με MRCC και MRCC ανθεκτικούς στη θεραπεία με MRCC, αντίστοιχα. Κυτοκίνες, και στην επιβίωση χωρίς εξέλιξη για ασθενείς με pNET.
Στρωματικοί όγκοι του γαστρεντερικού σωλήνα (GIST)
Μια αρχική κλιμάκωση ανοικτής ετικέτας διεξήχθη σε ασθενείς με GIST μετά από αποτυχία imatinib (μέση μέγιστη ημερήσια δόση 800 mg) λόγω αντοχής ή δυσανεξίας. Συμμετείχαν 97 ασθενείς με διαφορετικές δοσολογίες και δοσολογικά σχήματα. 55 ασθενείς έλαβαν θεραπεία με SUTENT 50 mg σύμφωνα με το συνιστώμενο πρόγραμμα 4 εβδομάδων φαρμάκου και δύο εβδομάδων απόσυρση φαρμάκου (πρόγραμμα 4/2).
Σε αυτή τη μελέτη, ο διάμεσος χρόνος για πρόοδο TTP ήταν 34,0 εβδομάδες (95% CI = 22,0-46,0 εβδομάδες).
Μια τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο μελέτη φάσης 3 της sunitinib διεξήχθη σε ασθενείς με GIST που είχαν δυσανεξία ή είχαν εξέλιξη της νόσου κατά τη διάρκεια ή μετά τη θεραπεία με imatinib (μέση μέγιστη ημερήσια δόση 800 mg). Σε αυτή τη μελέτη, 312 ασθενείς (2: 1) τυχαιοποιήθηκαν για να λάβουν 50 mg sunitinib ή εικονικό φάρμακο, από του στόματος μία φορά ημερησίως σύμφωνα με το πρόγραμμα 4/2 έως την εξέλιξη της νόσου ή την απόσυρση από τη μελέτη για «άλλο λόγο» (207 ασθενείς έλαβαν sunitinib και 105 εικονικό φάρμακο).
Το κύριο τελικό σημείο αποτελεσματικότητας της μελέτης ήταν το TTP, που ορίζεται ως ο χρόνος από την τυχαιοποίηση έως την πρώτη τεκμηρίωση της αντικειμενικής εξέλιξης του όγκου. Κατά τη στιγμή της προκαθορισμένης ενδιάμεσης ανάλυσης, ο διάμεσος TTP με sunitinib ήταν 28,9 εβδομάδες (95% CI = 21,3-34,1 εβδομάδες ) όταν αξιολογήθηκε από τον ερευνητή και 27,3 εβδομάδες (95% CI = 16,0-32,1 εβδομάδες) όταν αξιολογήθηκε από την Ανεξάρτητη Επιτροπή Ανασκόπησης και ήταν στατιστικά ανώτερο από το TTP 5,1 εβδομάδων που ελήφθη με εικονικό φάρμακο (95% CI = 4,4-10,1 εβδομάδες, Π
Ανεξάρτητη Επιτροπή Αναθεώρησης. Η διαφορά στη συνολική επιβίωση ήταν στατιστικά υπέρ της sunitinib [αναλογία κινδύνου: 0,491 95% (CI 0,290-0,831)]; ο κίνδυνος θανάτου ήταν 2 φορές υψηλότερος σε ασθενείς στο σκέλος του εικονικού φαρμάκου από εκείνους στον βραχίονα sunitinib.
Μετά την ενδιάμεση ανάλυση αποτελεσματικότητας και ασφάλειας, μετά από σύσταση του ανεξάρτητου DSMB, η μελέτη τυφλώθηκε και οι ασθενείς στο σκέλος του εικονικού φαρμάκου προσφέρθηκαν να στραφούν σε ανοικτού τύπου θεραπεία με sunitinib.
Συνολικά 255 ασθενείς έλαβαν θεραπεία με σουνιτινίμπη στη φάση ανοικτής θεραπείας της μελέτης, συμπεριλαμβανομένων 99 ασθενών που αρχικά έλαβαν εικονικό φάρμακο.
Η ανάλυση των πρωτογενών και δευτερογενών τελικών σημείων στη φάση ανοιχτής ετικέτας της μελέτης επιβεβαίωσε τα αποτελέσματα που ελήφθησαν κατά τη στιγμή της ενδιάμεσης ανάλυσης, όπως φαίνεται στον παρακάτω πίνακα.
Πίνακας 2 - Σύνοψη τελικών σημείων αποτελεσματικότητας (πληθυσμός ITT)
Η διάμεση συνολική επιβίωση (OS) στον πληθυσμό ITT ήταν 72,7 εβδομάδες και 64,9 εβδομάδες (HR 0,876, 95% CI 0,679 - 1,129, p = 0,306) στο σκέλος θεραπείας sunitinib και στο σκέλος εικονικού φαρμάκου, αντίστοιχα. Σε αυτήν την ανάλυση, το σκέλος του εικονικού φαρμάκου περιελάμβανε εκείνους τους ασθενείς που τυχαιοποιήθηκαν σε εικονικό φάρμακο και στη συνέχεια μεταπήδησαν σε ανοικτή θεραπεία με sunitinib.
Μεταστατικό καρκίνωμα νεφρικών κυττάρων (MRCC) σε ασθενείς που δεν είχαν λάβει προηγούμενη θεραπεία
Μια τυχαιοποιημένη, πολυκεντρική, διεθνής μελέτη φάσης 3 διεξήχθη για την αξιολόγηση της αποτελεσματικότητας και της ασφάλειας της σουνιτινίμπης σε σύγκριση με την ιντερφερόνη IFN-α σε ασθενείς που δεν είχαν λάβει προηγουμένως θεραπεία MRCC. Επτακόσιοι πενήντα ασθενείς τυχαιοποιήθηκαν 1: 1 στους βραχίονες θεραπείας. Έλαβαν θεραπεία sunitinib σε επαναλαμβανόμενοι κύκλοι 6 εβδομάδων. Κάθε κύκλος αποτελείται από 4 εβδομάδες με 50 mg ημερησίως από το στόμα, ακολουθούμενες από 2 εβδομάδες χωρίς λήψη του φαρμάκου (πρόγραμμα 4/2) ή με υποδόρια χορήγηση IFN-α σε δόση 3 εκατομμυρίων μονάδων (MU ) την πρώτη εβδομάδα, 6 MU τη δεύτερη εβδομάδα και από την τρίτη εβδομάδα και μετά σε δόση 9 MU σύμφωνα με θεραπεία 3 μη συνεχόμενων ημερών κάθε εβδομάδα.
Η μέση διάρκεια της θεραπείας ήταν 11,1 μήνες (εύρος: 0,4 - 46,1) για θεραπεία με sunitinib και 4,1 μήνες (εύρος 0,1 - 45,6) για θεραπεία με IFN -α.. Σοβαρές ανεπιθύμητες ενέργειες που σχετίζονται με τη θεραπεία (TRSAE) αναφέρθηκαν στο 23,7% των ασθενών που έλαβαν sunitinib και στο 6,9% των ασθενών που λάμβαναν IFN-α. Ωστόσο, τα ποσοστά διακοπής λόγω ανεπιθύμητων ενεργειών ήταν 20% για το sunitinib και 23% για το IFN-α. Διακοπές της θεραπείας συνέβησαν σε 202 ασθενείς (54%) στην ομάδα sunitinib και 141 ασθενείς (39%) στην ομάδα IFN-α.
Μειώσεις της δόσης σημειώθηκαν σε 194 ασθενείς (52%) που έλαβαν sunitinib και 98 ασθενείς (27%) που έλαβαν θεραπεία με IFN-α. Οι ασθενείς υποβλήθηκαν σε θεραπεία μέχρι την πρόοδο της νόσου ή την απόσυρση της μελέτης. Το κύριο τελικό σημείο αποτελεσματικότητας ήταν η επιβίωση χωρίς εξέλιξη (PFS).
Μια προγραμματισμένη ενδιάμεση ανάλυση έδειξε ένα στατιστικά σημαντικό πλεονέκτημα για το SUTENT έναντι του IFN-α. Σε αυτή τη μελέτη, ο διάμεσος PFS για την ομάδα sunitinib ήταν 47,3 εβδομάδες σε σύγκριση με 22,0 εβδομάδες για την ομάδα IFN-α. ο λόγος κινδύνου ήταν 0,415 (95% CI: 0,320-0,539, p-value
Η θεραπεία με Sunitinib συσχετίστηκε με μεγαλύτερη επιβίωση από τη θεραπεία με IFN-α. Η μέση συνολική επιβίωση ήταν 114,6 εβδομάδες για τον βραχίονα sunitinib (95% CI: 100,1 - 142,9 εβδομάδες) και 94,9 εβδομάδες για τον βραχίονα IFN -α (95% CI: 77,7 - 117,0 εβδομάδες) με αναλογία κινδύνου του 0,821 (95% CI: 0,673-1,001 · p = 0,0510 με βάση το μη στρωματοποιημένο τεστ καταγραφής).
Η επιβίωση χωρίς εξέλιξη (PFS) και η συνολική επιβίωση (OS), που παρατηρούνται στην πρόθεση θεραπείας του πληθυσμού (ITT) και προσδιορίζονται με ακτινολογική εργαστηριακή αξιολόγηση, συνοψίζονται στους ακόλουθους πίνακες:
Περίληψη των τελικών σημείων αποτελεσματικότητας (πληθυσμός ITT)
Ανθεκτικό σε κυτοκίνη μεταστατικό καρκίνωμα νεφρικών κυττάρων (MRCC)
Μια μελέτη φάσης 2 πραγματοποιήθηκε με το SUTENT σε ασθενείς ανθεκτικούς στην προηγούμενη θεραπεία με κυτοκίνη που έλαβαν θεραπεία με ιντερλευκίνη-2 ή IFN-α. Εξήντα τρεις ασθενείς έλαβαν από του στόματος αρχική δόση 50 mg sunitinib άπαξ ημερησίως για 4 συνεχόμενες εβδομάδες ακολουθούμενη από περίοδο 2 εβδομάδων ανάπαυσης για να ολοκληρώσουν μια πλήρη πορεία 6 εβδομάδων (πρόγραμμα θεραπείας 4/2). Το κύριο τελικό σημείο αποτελεσματικότητας ήταν το αντικειμενικό ποσοστό απόκρισης (Σκοπός
Ποσοστό απόκρισης (ORR)) σύμφωνα με τα κριτήρια RECIST (Κριτήρια αξιολόγησης απόκρισης σε στερεούς όγκους).
Σε αυτή τη μελέτη, το αντικειμενικό ποσοστό ανταπόκρισης ήταν 36,5% (95% CI 24,7% -49,6%) και ο διάμεσος χρόνος μέχρι την εξέλιξη (TTP) ήταν 37,7 εβδομάδες (95% CI 24,0-46,4 εβδομάδες).
Διεξήχθη μια ανοιχτή ετικέτα, πολυκεντρική, επιβεβαιωτική μελέτη για την αξιολόγηση της αποτελεσματικότητας και της ασφάλειας του sunitinib σε ασθενείς με MRCC ανθεκτικό στην προηγούμενη θεραπεία με κυτοκίνη. Εκατό έξι ασθενείς έλαβαν τουλάχιστον μία δόση 50 sunitinib. Mg σε πλαίσιο του σχεδίου 4/2.
Το κύριο τελικό σημείο αποτελεσματικότητας αυτής της μελέτης ήταν ο ρυθμός ORR. Τα δευτερεύοντα τελικά σημεία περιλάμβαναν TTP, διάρκεια απόκρισης (DR) και συνολική επιβίωση (OS).
Σε αυτή τη μελέτη, το ORR ήταν 35,8% (95% CI 26,8% -47,5%). Το DR και το μέσο λειτουργικό σύστημα δεν είχαν ακόμη επιτευχθεί.
Παγκρεατικοί νευροενδοκρινικοί όγκοι (pNET)
Μια ανοιχτή, πολυκεντρική, υποστηρικτική μελέτη φάσης 2 αξιολόγησε την αποτελεσματικότητα και την ασφάλεια της μονοθεραπείας sunitinib σε δόσεις 50 mg ημερησίως σε πρόγραμμα 4/2 [4 εβδομάδες θεραπείας, 2 εβδομάδες διακοπές] σε ασθενείς με μη λειτουργικό pNET Σε μια ομάδα 66 ασθενείς με καρκίνο κυττάρων νησιδίου του παγκρέατος το τελικό σημείο απόκρισης ήταν 17%.
Διεξήχθη μια κεντρική φάση 3, πολυκεντρική, διεθνής, τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο μελέτη μονοθεραπείας με sunitinib σε ασθενείς με μη χειρουργικό pNET.
Οι ασθενείς που έπρεπε να είχαν τεκμηριώσει την εξέλιξη της νόσου βάσει RECIST εντός των προηγούμενων 12 μηνών τυχαιοποιήθηκαν (1: 1) για να λάβουν 37,5 mg sunitinib άπαξ ημερησίως χωρίς προγραμματισμένη περίοδο απόσυρσης (n = 86) ή εικονικό φάρμακο (n = 85) Το
Το κύριο καταληκτικό σημείο ήταν η αξιολόγηση της επιβίωσης χωρίς εξέλιξη (PFS) σε ασθενείς που έλαβαν sunitinib έναντι εκείνων που λάμβαναν εικονικό φάρμακο. Άλλα τελικά σημεία ήταν το OS, το ποσοστό ORR, τα αποτελέσματα που αναφέρθηκαν από τον ασθενή) και η ασφάλεια.
Από την άποψη των δημογραφικών χαρακτηριστικών, οι ομάδες ασθενών που έλαβαν sunitinib και εικονικό φάρμακο ήταν συγκρίσιμες.Επιπλέον, το 49% των ασθενών που έλαβαν σουνιτινίμπη και το 52% των ασθενών που λάμβαναν εικονικό φάρμακο είχαν μη λειτουργικούς όγκους και το 92% των ασθενών και στα δύο χέρια είχαν μεταστάσεις στο ήπαρ. Η μελέτη επέτρεψε τη χρήση αναλόγων σωματοστατίνης. Το 66% των ασθενών που έλαβαν sunitinib και το 72% των ασθενών που έλαβαν εικονικό φάρμακο έλαβαν προηγουμένως συστηματική θεραπεία. Επιπλέον, το 24% των ασθενών στην ομάδα sunitinib και το 22% των ασθενών στο εικονικό φάρμακο η ομάδα έλαβε ανάλογα σωματοστατίνης. Ένα κλινικά σημαντικό πλεονέκτημα του sunitinib PFS σε σύγκριση με το εικονικό φάρμακο παρατηρήθηκε κατά την αξιολόγηση του ερευνητή. Το μέσο PFS ήταν 11,4 μήνες στο σκέλος sunitinib σε σύγκριση με 5, 5 μήνες στον βραχίονα του εικονικού φαρμάκου [λόγος κινδύνου: 0,418 (95% CI 0,263 , 0.662), p-value = 0.0001] · παρόμοια αποτελέσματα παρατηρήθηκαν όταν οι εκτιμήσεις της ανταπόκρισης του όγκου, με βάση την εφαρμογή του RECIST σε μετρήσεις του όγκου που πραγματοποιήθηκαν από τους ερευνητές, χρησιμοποιήθηκαν για τον προσδιορισμό της εξέλιξης της νόσου όπως φαίνεται στον Πίνακα 3. A αναλογία κινδύνου υπέρ της σουνιτινίμπης παρατηρήθηκε σε όλες τις υποομάδες που αξιολογήθηκαν για τα βασικά χαρακτηριστικά, συμπεριλαμβανομένης της ανάλυσης κατά αριθμό προηγούμενων συστηματικών θεραπειών. Συνολικά 29 ασθενείς στο σκέλος sunitinib και 24 στην ομάδα του εικονικού φαρμάκου δεν είχαν λάβει προηγούμενες συστηματικές θεραπείες · σε αυτούς τους ασθενείς εκεί »αναλογία κινδύνου για PFS ήταν 0,365 (95% CI 0,156, 0,857), p = 0,0156.
Ομοίως, μεταξύ των 57 ασθενών στον βραχίονα sunitinib (συμπεριλαμβανομένων 28 με 1 προηγούμενη συστηματική θεραπεία και 29 με 2 ή περισσότερες συστηματικές θεραπείες) και 61 ασθενείς στο σκέλος εικονικού φαρμάκου (συμπεριλαμβανομένων 25 με 1 προηγούμενη συστηματική θεραπεία και 36 με 2 ή περισσότερες συστηματικές θεραπείες ) l "αναλογία κινδύνου για PFS ήταν 0,456 (95% CI 0,264, 0,787), p = 0,0036.
Πραγματοποιήθηκε ανάλυση ευαισθησίας του PFS όταν το PFS βασίστηκε σε μετρήσεις του όγκου από ερευνητές και όταν όλα τα άτομα, που λογοκρίθηκαν για άλλους λόγους εκτός του τερματισμού της μελέτης, θεωρήθηκαν ότι ήταν συμβάντα PFS. Αυτή η ανάλυση παρείχε μια συντηρητική εκτίμηση της επίδρασης της θεραπείας με sunitinib και επιβεβαίωσε την πρωταρχική ανάλυση, αποδεικνύοντας ένα "αναλογία κινδύνου 0.507 (95% CI 0.350, 0.733), ρ = 0.000193. Η κεντρική μελέτη στο παγκρεατικό ΝΕΤ τερματίστηκε πρόωρα με βάση τη σύσταση μιας ανεξάρτητης επιτροπής αξιολόγησης φαρμάκων και το κύριο τελικό σημείο βασίστηκε στην αξιολόγηση του ερευνητή: και οι δύο καταστάσεις μπορεί να έχουν επηρεάσει την εκτίμηση του αποτελέσματος της θεραπείας.
Για να αποκλειστεί η προκατάληψη στην αξιολόγηση των PFS από τους ερευνητές, πραγματοποιήθηκε μια ανεξάρτητη, τυφλή κεντρική ανασκόπηση της διαγνωστικής απεικόνισης. αυτή η ανασκόπηση υποστήριξε την αξιολόγηση του ερευνητή, όπως φαίνεται στον Πίνακα 3.
Πίνακας 3 - Αποτελέσματα αποτελεσματικότητας από τη μελέτη pNET φάσης 3
CI = διάστημα εμπιστοσύνης, HR = λόγος κινδύνου, NA = Δεν ισχύει, NR = δεν έχει επιτευχθεί
ένα δίπλευρο τεστ μη στρωματοποιημένης καταγραφής
b Ακριβής δοκιμή Fisher
Ο συνολικός αριθμός επιβίωσης δεν ήταν ώριμος κατά τη διεξαγωγή της ανάλυσης. Υπήρχαν 9 θάνατοι στο σκέλος sunitinib και 21 θάνατοι στον βραχίονα του εικονικού φαρμάκου. Στατιστικά σημαντική διαφορά παρατηρήθηκε στο ποσοστό αντικειμενικής απόκρισης του sunitinib σε σύγκριση με το εικονικό φάρμακο.
Σε περιπτώσεις εξέλιξης της νόσου, οι ασθενείς ενημερώθηκαν για τη θεραπεία που λαμβάνουν και στους ασθενείς που έλαβαν εικονικό φάρμακο προσφέρθηκε η επιλογή να εγγραφούν σε διαφορετική ανοικτή ετικέτα επέκταση με sunitinib. Λόγω του πρώιμου τερματισμού της μελέτης, οι υπόλοιποι ασθενείς ενημερώθηκαν για τη θεραπεία που λαμβάνουν και τους προσφέρθηκε πρόσβαση σε μια ανοικτή μελέτη επέκτασης με sunitinib.Συνολικά 59 ασθενείς στο σκέλος του εικονικού φαρμάκου έλαβαν θεραπεία με sunitinib στη μελέτη. της επέκτασης.
Τα αποτελέσματα του Ερωτηματολογίου για την Ποιότητα Ζωής του Ευρωπαϊκού Οργανισμού Έρευνας και Θεραπείας του Καρκίνου (EORTC QLQ-C30) έδειξαν ότι η συνολική ποιότητα ζωής που σχετίζεται με την υγεία και οι πέντε λειτουργικοί τομείς (σωματικός, ρόλος, γνωστικός, συναισθηματικός και διατηρήθηκαν σε ασθενείς που έλαβαν σουνιτινίμπη, σε σύγκριση με εκείνους που λάμβαναν εικονικό φάρμακο, με λίγες συμπτωματικές παρενέργειες.
Παιδιατρικός πληθυσμός
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων ανέβαλε την υποχρέωση υποβολής των αποτελεσμάτων των μελετών με το SUTENT σε ένα ή περισσότερα υποσύνολα του παιδιατρικού πληθυσμού για τη θεραπεία των GIST (βλ. Παράγραφο 4.2 για πληροφορίες σχετικά με την παιδιατρική χρήση).
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων έχει παραιτηθεί από την υποχρέωση υποβολής των αποτελεσμάτων των μελετών με το SUTENT σε όλα τα υποσύνολα του παιδιατρικού πληθυσμού για τη θεραπεία νεφρικών και νεφρικών πυελικών καρκινωμάτων (με εξαίρεση το νεφροβλάστωμα, τη νεφροβλαστομάτωση, το διαυγές σάρκωμα, το μεσοβλαστικό νεφρώμα, το μυελικό νεφρό) καρκίνωμα και ραβδοειδής όγκος του νεφρού) (βλ. παράγραφο 4.2 για πληροφορίες σχετικά με την παιδιατρική χρήση).
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων έχει παραιτηθεί από την υποχρέωση υποβολής των αποτελεσμάτων των μελετών με το SUTENT σε όλα τα υποσύνολα του παιδιατρικού πληθυσμού για τη θεραπεία γαστρεντεροπαγκρεατικών νευροενδοκρινών όγκων (με εξαίρεση το νευροβλάστωμα, το νευροαγγλιοβλάστωμα, το φαιοχρωμοκύτωμα) (βλ. Παράγραφο 4.2 για πληροφορίες σχετικά με την παιδιατρική χρήση ).
05.2 "Φαρμακοκινητικές ιδιότητες
Η φαρμακοκινητική της sunitinib αξιολογήθηκε σε 135 υγιείς εθελοντές και σε 266 ασθενείς με συμπαγείς όγκους. Η φαρμακοκινητική ήταν παρόμοια σε όλους τους πληθυσμούς ασθενών με συμπαγή όγκο που δοκιμάστηκαν και σε υγιείς εθελοντές.
Μέσα στα δοσολογικά σχήματα των 25-100 mg, η περιοχή κάτω από την καμπύλη (AUC) και η Cmax αυξάνονται ανάλογα με τη δόση. Με επαναλαμβανόμενη ημερήσια χορήγηση, το sunitinib συσσωρεύεται 3-4 φορές και ο κύριος ενεργός μεταβολίτης συσσωρεύεται 7-10 φορές. Οι συγκεντρώσεις σταθερής κατάστασης της σουνιτινίμπης και του κύριου ενεργού μεταβολίτη της επιτυγχάνονται εντός 10-14 ημερών. Μέχρι την 14η ημέρα, οι συνδυασμένες συγκεντρώσεις του sunitinib στο πλάσμα και ο κύριος ενεργός μεταβολίτης του είναι 62,9 - 101 ng / mL και αντιπροσωπεύουν τις προβλεπόμενες συγκεντρώσεις στόχους με βάση τα προκλινικά δεδομένα για την αναστολή της φωσφορυλίωσης των υποδοχέων. in vitro και οδηγούν σε μείωση της στάσης / ανάπτυξης του όγκου in vivo.
Ο κύριος ενεργός μεταβολίτης αντιπροσωπεύει το 23-37% της συνολικής έκθεσης στο φάρμακο. Δεν παρατηρούνται σημαντικές αλλαγές στη φαρμακοκινητική του sunitinib ή του κύριου δραστικού μεταβολίτη με επαναλαμβανόμενες θεραπείες άπαξ ημερησίως ή επαναλαμβανόμενες δοσολογίες.
Απορρόφηση
Μετά την από του στόματος χορήγηση sunitinib, οι μέγιστες συγκεντρώσεις (Cmax) παρατηρούνται γενικά εντός 6-12 ωρών (Tmax) από την πρόσληψη φαρμάκου.
Τα τρόφιμα δεν έχουν καμία επίδραση στη βιοδιαθεσιμότητα του sunitinib.
Κατανομή
Η δέσμευση της σουνιτινίμπης και του κύριου ενεργού μεταβολίτη της στις ανθρώπινες πρωτεΐνες πλάσματος σε δοκιμές σε in vitro ήταν 95% και 90%, αντίστοιχα, χωρίς «εμφανή εξάρτηση από τη συγκέντρωση.
Ο φαινομενικός όγκος κατανομής (Vd) του sunitinib ήταν μεγάλος - 2.230 l - υποδεικνύοντας την κατανομή στους ιστούς.
Μεταβολικές αλληλεπιδράσεις
Οι υπολογισμένες τιμές Ki in vitro για όλες τις ισομορφές κυτταροχρώματος (CYP) ο μεταβολισμός άλλων δραστικών ουσιών που μπορούν να μεταβολιστούν από αυτά τα ένζυμα.
Βιομετασχηματισμός
Το Sunitinib μεταβολίζεται κυρίως από το CYP3A4, το ισόμορφο του κυτοχρώματος P450, το οποίο παράγει τον κύριο ενεργό μεταβολίτη του, το desethyl sunitinib, το οποίο μεταβολίζεται περαιτέρω από το ίδιο ισοένζυμο.
Η συγχορήγηση σουνιτινίμπης και ισχυρών επαγωγέων ή αναστολέων του CYP3A4 θα πρέπει να αποφεύγεται επειδή τα επίπεδα της σουνιτινίμπης στο πλάσμα μπορεί να μεταβληθούν (βλέπε παραγράφους 4.4 και 4.5).
Εξάλειψη
Η απέκκριση πραγματοποιείται κυρίως μέσω κοπράνων (61%) και νεφρική αποβολή της αμετάβλητης δραστικής ουσίας και των μεταβολιτών της αντιπροσωπεύει το 16% της χορηγούμενης δόσης.Το Sunitinib και ο κύριος ενεργός μεταβολίτης του ήταν οι κύριες ενώσεις που εντοπίστηκαν στο πλάσμα, τα ούρα και τα κόπρανα και αντιπροσώπευαν το 91,5%, το 86,4%και το 73,8%, αντίστοιχα, της ραδιενέργειας που ανιχνεύθηκε στα συγκεντρωμένα δείγματα. Μικροί μεταβολίτες έχουν εντοπιστεί στα ούρα και τα κόπρανα, αλλά γενικά δεν έχουν εντοπιστεί στο πλάσμα. Η συνολική κάθαρση από το στόμα (CL / F) ήταν 34-62 L / h.
Μετά από από του στόματος χορήγηση σε υγιείς εθελοντές, ο χρόνος ημίσειας ζωής αποβολής του sunitinib και του κύριου ενεργού μεταβολίτη του desethyl είναι περίπου 40-60 ώρες και 80-110 ώρες, αντίστοιχα.
Ειδικοί πληθυσμοί
Ηπατική δυσλειτουργία: Το Sunitinib και ο κύριος μεταβολίτης του μεταβολίζονται κυρίως από το ήπαρ. Οι συστηματικές εκθέσεις μετά από μία μόνο δόση sunitinib ήταν παρόμοιες σε άτομα με ήπια ή μέτρια ηπατική δυσλειτουργία (στάδια Α και Β Child-Pugh) σε σύγκριση με άτομα με φυσιολογική ηπατική λειτουργία. Το SUTENT δεν έχει μελετηθεί σε άτομα με σοβαρή ηπατική δυσλειτουργία (στάδιο C-Child-Pugh).
Μελέτες για τον καρκίνο απέκλεισαν ασθενείς με ALT ή AST> 2,5 x ULN (ανώτερο φυσιολογικό όριο) ή εάν αυτές οι τιμές ήταν> 5,0 x ULN λόγω ηπατικών μεταστάσεων.
Νεφρική δυσλειτουργία: Φαρμακοκινητικές αναλύσεις πληθυσμού έδειξαν ότι η φαινομενική κάθαρση της sunitinib (CL / F) δεν επηρεάστηκε από την κάθαρση κρεατινίνης στο εύρος που εξετάστηκε (42-347 mL / min). Η συστηματική έκθεση μετά από μία μόνο δόση sunitinib ήταν παρόμοια σε άτομα με σοβαρή νεφρική δυσλειτουργία ( Αν και η σουνιτινίμπη και ο κύριος μεταβολίτης της δεν καθαρίστηκαν με αιμοκάθαρση σε άτομα με ESRD, η συνολική συστηματική έκθεση ήταν 47% χαμηλότερη για τη σουνιτινίμπη και 31% για τον κύριο μεταβολίτη της σε σύγκριση με άτομα με φυσιολογική νεφρική λειτουργία.
Βάρος, κατάσταση απόδοσης: Οι πληθυσμιακές φαρμακοκινητικές αναλύσεις δείχνουν ότι δεν απαιτούνται προσαρμογές της αρχικής δόσης για το βάρος και την κατάσταση απόδοσης της Eastern Cooperative Oncology Group (ECOG).
Φύλο του ανήκειν: Τα διαθέσιμα δεδομένα υποδεικνύουν ότι τα θηλυκά μπορεί να έχουν 30% χαμηλότερη φαινόμενη κάθαρση sunitinib (CL / F) από τα αρσενικά. αυτή η διαφορά, ωστόσο, δεν απαιτεί προσαρμογές της αρχικής δόσης.
05.3 Προκλινικά δεδομένα ασφάλειας
Μελέτες τοξικότητας επαναλαμβανόμενων δόσεων σε αρουραίους και πιθήκους διάρκειας έως 9 μηνών έδειξαν ότι οι κύριες επιδράσεις των οργάνων -στόχων είναι στο γαστρεντερικό σωλήνα (έμετος και διάρροια σε πιθήκους). τα επινεφρίδια (συμφόρηση του φλοιού ή / και αιμορραγία σε αρουραίους και πιθήκους, με νέκρωση που ακολουθείται από ίνωση σε αρουραίους) · το αίμα και το λεμφικό σύστημα (υποκυτταρικότητα μυελού των οστών και λεμφοειδής εξάντληση του θύμου αδένα, της σπλήνας και των λεμφαδένων) · το εξωκρινές πάγκρεας (αποκοκκιοποίηση κυττάρων acinar με νέκρωση κυττάρων) τους σιελογόνους αδένες (υπερτροφία του κοκίνου). οστικές αρθρώσεις (πάχυνση της πλάκας ανάπτυξης). μήτρα (ατροφία) και ωοθήκες (μείωση της ανάπτυξης των ωοθυλακίων). Όλα τα αποτελέσματα εμφανίστηκαν με κλινικά σχετικά επίπεδα έκθεσης στο sunitinib στο πλάσμα. Άλλες επιδράσεις που παρατηρήθηκαν στις μελέτες περιελάμβαναν: παράταση του διαστήματος QTc, μείωση του κλάσματος εξώθησης της αριστερής κοιλίας (LVEF) και όρχεις σωληνοειδής ατροφία, αυξημένα μεσαγγειακά κύτταρα στο νεφρό, αιμορραγία του γαστρεντερικού σωλήνα και του βλεννογόνου του στόματος και υπερτροφία των πρόσθιων κυττάρων της υπόφυσης. ενδομήτριο) και πλάκα ανάπτυξης οστών (επιφυσιακή πάχυνση ή δυσπλασία χόνδρου) σχετίζονται με τη φαρμακολογική δράση του sunitinib. Τα περισσότερα από αυτά τα συμβάντα ήταν αναστρέψιμα μετά τη διακοπή της θεραπείας για 2-6 εβδομάδες.
Γονοτοξικότητα
Το γονοτοξικό δυναμικό της sunitinib αξιολογήθηκε in vitro και in vivoΤο Το Sunitinib δεν παρουσίασε μεταλλαξιογόνες επιδράσεις σε βακτήρια χρησιμοποιώντας τη μεταβολική ενεργοποίηση που παρέχεται από το ήπαρ του αρουραίου. Το Sunitinib δεν προκάλεσε δομικές χρωμοσωμικές αποκλίσεις στα ανθρώπινα περιφερικά λεμφοκύτταρα in vitroΤο Πολυπλοειδία (αποκλίσεις σε αριθμό χρωμοσωμάτων) έχει παρατηρηθεί σε ανθρώπινα περιφερικά λεμφοκύτταρα σε in vitro, παρουσία και απουσία μεταβολικής ενεργοποίησης. Το Sunitinib δεν έδειξε καμία πιθανότητα κλαστογένεσης στον μυελό των οστών αρουραίου in vivo. Ο κύριος ενεργός μεταβολίτης δεν έχει αξιολογηθεί ως προς το γονοτοξικό δυναμικό.
Καρκινογένεση
Στη μελέτη 1 μηνός για να βρεθεί το εύρος δόσεων (0, 10, 25, 75, ή 200 mg / kg / ημέρα) στο οποίο τα διαγονιδιακά ποντίκια rasH2 τροφοδοτήθηκαν με έναν από του στόματος ιχνηλάτη με δοσολογία καθημερινά και συνεχώς τη δόση όταν χορηγήθηκε, σε παρατηρήθηκαν οι υψηλότερες δόσεις (200 mg / kg / ημέρα) καρκινώματος και υπερπλασίας των αδένων του Brunner στο δωδεκαδάκτυλο.
Μια μελέτη διάρκειας 6 μηνών διεξήχθη για την αξιολόγηση της καρκινογένεσης σε διαγονιδιακά ποντίκια rasH2 που τροφοδοτήθηκαν με στοματικό σωλήνα με δοσολογία της χορηγούμενης δόσης καθημερινά (0, 8, 25, 75 [μειωμένη σε 50] mg / kg / ημέρα). Σε δόσεις ≥25 mg / kg / ημέρα χορηγούμενες για 1 ή 6 μήνες (≥7,3 φορές την AUC που παρατηρήθηκε σε ασθενείς που έλαβαν τη συνιστώμενη ημερήσια δόση [RDD]), γαστροδωδεκαδακτυλικό καρκίνωμα, παρατηρήθηκε αυξημένη συχνότητα εμφάνισης. Αιμαγγειοσάρκωμα και / ή υπερπλασία ο γαστρικός βλεννογόνος.
Σε μια διετή μελέτη για την αξιολόγηση της καρκινογένεσης σε αρουραίους (0, 0,33, 1 ή 3 mg / kg / ημέρα) όταν η sunitinib χορηγήθηκε σε κύκλους 28 ημερών ακολουθούμενη από περιόδους 7 ημερών χωρίς χορήγηση, διαπιστώθηκε αύξηση της συχνότητας φαιοχρωμοκύτωμα και μυελική υπερπλασία των επινεφριδίων σε αρσενικούς αρουραίους που είχαν λάβει δόση 3 mg / kg / ημέρα για περισσότερο από 1 έτος (≥ 7,8 φορές την AUC σε ασθενείς που έλαβαν RDD). Το καρκίνωμα του αδένα Brunner εμφανίστηκε στο δωδεκαδάκτυλο σε δόσεις ≥ 1 mg / kg / ημέρα στις γυναίκες, σε δόσεις 3 mg / kg / ημέρα σε άνδρες και η υπερπλασία των βλεννογόνων ήταν εμφανής στους στοματικούς αδένες σε ίσες δόσεις. Στα 3 mg / kg / ημέρα στους άνδρες · αυτά τα συμβάντα εμφανίστηκαν σε δόσεις 0,9, 7,8 και 7,8 φορές της AUC σε ασθενείς που λάμβαναν ΣΑΠ, αντίστοιχα. Η συνάφεια αυτών των νεοπλαστικών ευρημάτων που παρατηρήθηκαν σε μελέτες καρκινογένεσης σε ποντίκια (rasH2) και αρουραίους σε ανθρώπους που έλαβαν sunitinib είναι αβέβαιη.
Τοξικότητα για την αναπαραγωγή και την ανάπτυξη
Δεν παρατηρήθηκαν επιδράσεις στη γονιμότητα των ανδρών ή των γυναικών σε μελέτες τοξικότητας στην αναπαραγωγή. Ωστόσο, μελέτες τοξικότητας επαναλαμβανόμενων δόσεων που διεξήχθησαν σε αρουραίους και πιθήκους έδειξαν επιδράσεις στη γυναικεία γονιμότητα με τη μορφή ωοθυλακικής ατρησίας, εκφυλισμού του ωχρού σώματος, μεταβολών του ενδομητρίου στη μήτρα και μείωσης του βάρους της μήτρας και των ωοθηκών σε επίπεδα κλινικά συναφή συστημική έκθεση. Επιδράσεις στη γονιμότητα των αρσενικών αρουραίων παρατηρήθηκαν με τη μορφή σωληνοειδούς ατροφίας στους όρχεις, μειωμένων σπερματοζωαρίων στην επιδιδυμίδα και κολλοειδούς εξάντλησης στον προστάτη και σπερματικών κυστιδίων σε επίπεδα έκθεσης στο πλάσμα 25 φορές περισσότερο από την ανθρώπινη συστηματική έκθεση.
Σε αρουραίους, η εμβρυϊκή θνησιμότητα οδήγησε σε σημαντική μείωση του αριθμού των ζωντανών εμβρύων, αυξημένο αριθμό απορροφήσεων, αυξημένες απώλειες μετά την εμφύτευση και συνολικές απώλειες απογόνων σε 8 από τις 28 έγκυες γυναίκες σε επίπεδα έκθεσης στο πλάσμα 5,5 φορές τη συστηματική έκθεση στους ανθρώπους Το Στα κουνέλια, η μείωση του βάρους της εγκύου μήτρας και ο αριθμός των ζωντανών εμβρύων προκλήθηκαν από την αύξηση των απορροφήσεων του εμβρύου, τις απώλειες μετά την εμφύτευση και τις συνολικές απώλειες απογόνων σε 4 από τις 6 έγκυες γυναίκες σε επίπεδα τριπλάσιας έκθεσης στο πλάσμα. στους ανθρώπους. Η θεραπεία με σουνιτινίμπη σε αρουραίους κατά τη διάρκεια της οργανογένεσης είχε ως αποτέλεσμα αναπτυξιακές επιδράσεις σε δόσεις ≥ 5 mg / kg / ημέρα, που αποτελούνται από αυξημένη συχνότητα εμβρυϊκών σκελετικών δυσπλασιών, που χαρακτηρίζονται κυρίως από καθυστερημένη οστεοποίηση των θωρακικών / οσφυϊκών σπονδύλων και εμφανίζονται σε επίπεδα έκθεσης στο πλάσμα 5,5 φορές την ανθρώπινη συστηματική έκθεση. Στα κουνέλια, οι αναπτυξιακές επιδράσεις συνίστανται σε αυξημένη συχνότητα σχισμών στα χείλη σε επίπεδα έκθεσης στο πλάσμα περίπου ίσα με αυτά που παρατηρήθηκαν στην κλινική, και σχισμής χείλους και ουρανίσκου σε επίπεδα έκθεσης στο πλάσμα 2,7 φορές τη συστηματική έκθεση στον άνθρωπο.
Οι επιδράσεις της σουνιτινίμπης (0,3, 1,0, 3,0 mg / kg / ημέρα) στην προ και μεταγεννητική ανάπτυξη αξιολογήθηκαν σε μια μελέτη σε έγκυες θηλυκές αρουραίους. Η αύξηση του σωματικού βάρους της μητέρας κατά τη διάρκεια της κύησης και της γαλουχίας μειώθηκε σε δόσεις> 1 mg / kg / ημέρα, αλλά δεν παρατηρήθηκε τοξικότητα στη μητρική αναπαραγωγική έως τις δόσεις των 3 mg / kg / ημέρα (εκτιμώμενη έκθεση> 2, 3 φορές η AUC που παρατηρήθηκε σε ασθενείς λήψη RDD) Παρατηρήθηκαν μειωμένα σωματικά βάρη απογόνων σε δόσεις 3 mg / kg / ημέρα στις περιόδους πριν και μετά τον απογαλακτισμό.Δεν παρατηρήθηκε αναπτυξιακή τοξικότητα σε δόσεις 1 mg / kg / ημέρα (έκθεση περίπου. 0,9 φορές την AUC που παρατηρήθηκε σε ασθενείς που λάμβαναν RDD).
06.0 ΦΑΡΜΑΚΕΥΤΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ
06.1 Έκδοχα
Περιεχόμενα κάψουλας
Μαννιτόλη (E421)
Νάτριο κροσκαρμελόζη
Ποβιδόνη (Κ-25)
Στεατικό μαγνήσιο
Κέλυφος κάψουλας
Πηκτή
Κόκκινο οξείδιο του σιδήρου (E172)
Διοξείδιο του τιτανίου (E171)
Μελάνι
Γομμαλάκα
Προπυλενογλυκόλη
Υδροξείδιο του νατρίου
Ποβιδόνη
Διοξείδιο του τιτανίου (E171)
06.2 Ασυμβατότητα
Ασχετο.
06.3 Περίοδος ισχύος
3 χρόνια.
06.4 Ειδικές προφυλάξεις κατά την αποθήκευση
Αυτό το φαρμακευτικό προϊόν δεν απαιτεί ειδικές συνθήκες φύλαξης.
06.5 Φύση της άμεσης συσκευασίας και περιεχόμενο της συσκευασίας
Μπουκάλια πολυαιθυλενίου υψηλής πυκνότητας (HDPE), με κλείσιμο από πολυπροπυλένιο, που περιέχουν 30 σκληρά καψάκια.
Διαφανείς φουσκάλες από πολυ (χλωροτριφθοροαιθυλένιο) / PVC με διάτρητες μοναδιαίες δόσεις και με φύλλο αλουμινίου με βερνίκι θερμικής σφράγισης που περιέχει 28 x 1 σκληρά καψάκια.
Μπορεί να μην κυκλοφορούν όλες οι συσκευασίες.
06.6 Οδηγίες χρήσης και χειρισμού
Χωρίς ειδικές οδηγίες.
07.0 ΚΑΤΟΧΟΣ ΑΔΕΙΑΣ ΜΑΡΚΕΤΙΝΓΚ
Pfizer Ltd
Ramsgate Road
Sandwich, Kent CT13 9NJ
Ηνωμένο Βασίλειο
08.0 ΑΡΙΘΜΟΣ ΑΔΕΙΑΣ ΜΑΡΚΕΤΙΝΓΚ
ΕΕ/1/06/347/001
037192022
ΕΕ/1/06/347/004
09.0 ΗΜΕΡΟΜΗΝΙΑ ΠΡΩΤΗΣ ΕΓΚΡΙΣΗΣ ΑΝΑΝΕΩΣΗΣ ΤΗΣ ΑΔΕΙΑΣ
Ημερομηνία πρώτης έγκρισης: 19 Ιουλίου 2006
Ημερομηνία πρόσφατης ανανέωσης: 09 Ιανουαρίου 2012
10.0 ΗΜΕΡΟΜΗΝΙΑ ΑΝΑΘΕΩΡΗΣΗΣ ΤΟΥ ΚΕΙΜΕΝΟΥ
11.0 ΓΙΑ ΡΑΔΙΟΦΑΡΜΑΚΑ, ΟΛΟΚΛΗΡΩΜΕΝΑ ΔΕΔΟΜΕΝΑ ΣΤΗΝ ΕΣΩΤΕΡΙΚΗ ΔΟΣΟΜΕΤΡΙΑ ΑΚΤΙΝΟΒΟΛΙΑΣ
12.0 ΓΙΑ ΡΑΔΙΟΦΑΡΜΑΚΑ ΦΑΡΜΑΚΑ, ΠΡΟΣΘΕΤΕΣ ΛΕΠΤΟΜΕΡΕΙΕΣ ΟΔΗΓΙΕΣ ΣΧΕΤΙΚΑ ΜΕ ΕΛΕΓΧΟ ΠΡΟΕΤΟΙΜΑΣΙΑΣ ΚΑΙ ΠΟΙΟΤΗΤΑΣ